Журнал «Почки» Том 14, №3, 2025
Вернуться к номеру
Дисфункція ендотелію та зниження швидкості клубочкової фільтрації в осіб різного віку з ознаками кардіоренометаболічного синдрому: шляхи ангіо- та ренопротекції
Авторы: Чижова В.П. (1, 2), Дужак Г.В. (1), Самоць І.А. (1), Ковтонюк Т.І. (1), Богомаз Л.М. (1), Диба І.А. (1), Табакович-Вацеба В.О. (1), Гриб О.М. (1), Кононенко О.А. (2), Серебровська З.О. (1), Толстун Д.О. (1), Сикало Н.В. (1), Фархідінов І.О. (1), Кропива В. (1), Мигован С.А. (1), Маньковський Б.М. (1, 2)
(1) - ДУ «Інститут геронтології ім. Д.Ф. Чеботарьова» НАМН України, м. Київ, Україна
(2) - Національний університет охорони здоров’я України ім. П.Л. Шупика, м. Київ, Україна
Рубрики: Нефрология
Разделы: Клинические исследования
Версия для печати
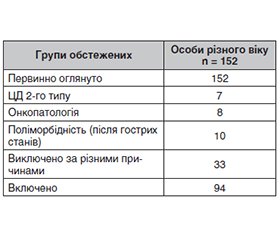
Актуальність. Кардіоренометаболічний синдром (КРМС) — це сукупність патологічних станів, які поєднують метаболічні порушення, серцево-судинну дисфункцію та ураження нирок, формуючи взаємопов’язану систему ускладнень. Особливу роль у розвитку та прогресуванні цього синдрому відіграє ендотеліальна дисфункція — ранній маркер судинного ураження, що асоціюється з порушенням вазодилатації, хронічним запаленням та проатерогенними змінами. Водночас зниження показника розрахункової швидкості клубочкової фільтрації (рШКФ) відображає не лише функціональний стан нирок, а й загальний ризик серцево-судинних подій та смертності. У контексті старіння популяції та зростання поширеності КРМС серед осіб різного віку, особливо середнього й похилого, актуальним стає вивчення взаємозв’язку між дисфункцією ендотелію та зниженням рШКФ. Рання діагностика цих порушень дозволить не лише виявити осіб з високим кардіоренальним ризиком, а й впровадити підходи до профілактики, ранньої діагностики та лікування. Мета: оцінити функціональний стан нирок і судинного ендотелію в осіб різного віку з ознаками КРМС та з’ясувати можливості корекції виявлених змін застосуванням екстракту леспедези головчастої (Lespedeza capitata) як потенційного засобу нефро- та ангіопротекції. Матеріали та методи. Первинно обстежено 152 особи різного віку. Згідно з критеріями включення було виключено 58 осіб за різними причинами. Комплексне обстеження проведено у 94 осіб різного віку (середній вік становив 54,82 ± 0,97 року), з яких у більшості виявлено зниження рШКФ, підвищення співвідношення альбумін/креатинін (САК) у сечі та зниження функції ендотелію. Для корекції виявлених змін на фоні проведення стандартної антигіпертензивної терапії було додано до лікування Lespedeza capitata, яку призначали незалежно від прийому їжі протягом 1 місяця попередньо обстеженим особам (n = 39). Критеріями ефективності лікування були: динаміка рШКФ, САК у сечі та показники функціонального стану ендотелію (приріст кровотоку при проведенні проби з реактивною гіперемією). Термін спостереження за пацієнтами становив 1 місяць. Обстеження проводили з використанням стандартних клінічних, антропометричних, лабораторних і інструментальних методів. Результати. З віком відмічається тенденція до зниження показника рШКФ з 79,73 ± 1,91 мл/хв/1,73 м2 у середньому віці (47,28 ± 0,72 року) до 64,01 ± 2,21 мл/хв/1,73 м2 у похилому віці (67,18 ± 0,49 року). В осіб середнього віку (100 %) рШКФ знаходиться в межах категорії G2 (60–89 мл/хв/1,73 м2), водночас у 46 % осіб похилого віку рШКФ знижується до категорії G3а (45–59 мл/хв/1,73 м2). Нормальна або висока рШКФ (категорія G1, ≥ 90 мл/хв/1,73 м2) зберігається лише у 10 % обстежених похилого віку. Серед осіб середнього віку із незначним зниженням рШКФ у межах категорії G2 (60–89 мл/хв/1,73 м2) виявлено підвищення показника САК у третини обстежених, тоді як в осіб похилого віку превалює зниження рШКФ до 40–59 мл/хв/1,73 м2, яке розцінюється як хронічна хвороба нирок (ХХН) у межах категорії G3а, що супроводжується підвищенням показника САК у 25 % осіб. При оцінці функціонального стану ендотелію великих судин виявлено, що серед обстежених осіб (n = 94) з різними категоріями рШКФ (G1, G2, G3а) ознаки ендотеліальної дисфункції спостерігалися у 54 хворих (57,45 %). Із них у 19 пацієнтів (35,18 %) зафіксовано крайній ступінь порушення — вазоспастичну реакцію при проведенні проби за методикою D.S. Celermajer, що свідчить про виражене порушення ендотелійзалежної вазодилатації. Серед обстежених осіб із дисфункцією ендотелію великих судин у 70,4 % (38 осіб) показник САК виявився < 30 мг/г, в 29,6 % (16 осіб) виявилося підвищене САК (у 10 осіб — 30–300 мг/г, а у 6 осіб — понад 300 мг/г). Водночас у групі осіб із збереженою функцією ендотелію були такі показники: у 65 % (26 осіб) САК виявлено на рівні < 30 мг/г, у 14 осіб САК становило 30–300 мг/г, не виявлено осіб з САК понад 300 мг/г. Таким чином, лише серед пацієнтів з ендотеліальною дисфункцією зафіксовано САК > 300 мг/г (у 5 осіб, або 9,2 %), що демонструє вірогідну статистичну різницю (χ2 = 0,01, p = 0,03). Серед осіб зі зниженням рШКФ у межах категорії G2 (60–89 мл/хв/1,73 м2) та G3а (45–59 мл/хв/1,73 м2) відмічено зниження ендотеліальної функції судин мікроциркуляторної ланки у 84 % обстежених, при цьому САК < 30 мг/г виявлено у 50,00 %, САК в межах 30–300 мг/г виявлено у 43,75 %, САК понад 300 мг — у 6,25 % порівняно з групою осіб (16 %) зі збереженою функцією судин мікроциркуляторної ланки: 33,30; 66,70 % відповідно за відсутності осіб із САК понад 300 мг/г. Ця тенденція невірогідна (χ2 = 0,08, р = 0,13), проте повторює таку ж тенденцію щодо наявності показника САК понад 300 мг/г в осіб із порушенням функціонального стану ендотелію великих судин. Потрібно відмітити наявність феномену взаємообтяження в осіб зі зниженою рШКФ в межах 45–89 мл/хв/1,73 м2. Так, 56,25 % обстежених мають поєднання дисфункції ендотелію великих та дрібних судин, з них у 44,44 % відмічено показник САК 30–300 мг/г і у 11,11 % — САК понад 300 мг/г. Відсутність осіб із рівнем САК > 300 мг/г серед пацієнтів зі збереженою ендотеліальною функцією (як у середньому, так і в похилому віці) свідчить про тісний зв’язок між значною альбумінурією та ендотеліальною дисфункцією. Імовірно, САК > 300 мг/г можна розглядати як індикатор значного пошкодження судинної стінки, який відображає наявність системної ендотеліальної дисфункції. З метою корекції виявлених змін 39 особам різного віку з проявами КРМС до стандартної антигіпертензивної терапії було призначено екстракт леспедези головчастої (Lespedeza capitata). У всіх обстежених пацієнтів через 1 місяць стандартної терапії, доповненої екстрактом леспедези головчастої (Lespedeza capitata), збільшився показник приросту кровотоку, що свідчить про відновлення функціонального стану ендотелію великих судин та судин мікроциркуляторної ланки. На фоні відновлення функціонального стану ендотелію відмічена стійка тенденція до збільшення частки осіб із показником САК< 30 мг/г (χ2 = 0,04, р = 0,07), що свідчить про відновлення функціонального стану нирок. Такий ефект зумовлений тим, що екстракти з пагонів леспедези головчастої характеризуються доведеною нефропротекторною дією, що дозволяє використовувати їх для профілактики та лікування ХХН. Висновки. У осіб різного віку з проявами КРМС наявний феномен взаємообтяження: у понад половини пацієнтів із рШКФ 45–89 мл/хв/1,73 м2 (56,25 %) виявлено поєднану дисфункцію ендотелію як дрібних, так і великих судин, що супроводжується підвищеним рівнем САК (у 11,11 % — > 300 мг/г). Отримані дані свідчать про важливу роль підвищення показника САК як потенційного маркера ендотеліальної дисфункції на ранніх стадіях зниження функції нирок: високий рівень САК може виступати маркером наявного пошкодження ендотелію, тоді як низькі чи помірні значення (САК < 30 мг/г або 30–300 мг/г) ще можуть спостерігатися на фоні збереженої функції ендотелію. З метою ангіо- та нефропротекції в осіб з КРМС доцільно до стандартної антигіпертензивної терапії додавати екстракт леспедези головчастої (Lespedeza capitata).
Background. Cardio-renal-metabolic syndrome (CRMS) is a cluster of pathological conditions that combine metabolic disorders, cardiovascular dysfunction, and kidney damage, forming an interconnected system of complications. Endothelial dysfunction plays a key role in the development and progression of this syndrome as an early marker of vascular damage associated with impaired vasodilation, chronic inflammation, and pro-atherogenic changes. At the same time, a decrease in the estimated glomerular filtration rate (eGFR) reflects not only kidney function but also the overall risk of cardiovascular events and mortality. Given the population aging and the increasing prevalence of CRMS among individuals of various age groups, especially middle-aged and elderly, studying the relationship between endothelial dysfunction and reduced eGFR is highly relevant. Early diagnosis of these changes may allow timely identification of individuals at high cardiorenal risk and implementation of approaches to the prevention, early detection, and treatment. The purpose was to assess kidney function and vascular endothelial status in individuals of different age groups with signs of CRMS and to evaluate the potential for correction of the detected changes using Lespedeza capitata extract as a potential nephro- and angioprotective agent. Materials and methods. A total of 152 individuals of various ages were initially examined. Based on inclusion criteria, 58 people were excluded for various reasons. Comprehensive examination was carried out in 94 individuals (mean age of 54.82 ± 0.97 years), most of them demonstrated decreased eGFR, elevated urinary albumin-to-creatinine ratio (UACR), and impaired endothelial function. To correct these changes, Lespedeza capitata extract was added to standard antihypertensive therapy. The supplement was administered at a dose of one capsule three times daily regardless of meals, for one month, to pre-screened individuals (n = 39). Effectiveness criteria included changes in eGFR, UACR, and markers of endothelial function (flow-mediated dilation assessed by reactive hyperemia). The observation period was one month. The examination included standard clinical, anthropometric, laboratory, and instrumental methods. Results. With age, a tendency toward decreased eGFR was observed: from 79.73 ± 1.91 mL/min/1.73 m2 in middle-aged individuals (47.28 ± 0.72 years) to 64.01 ± 2.21 mL/min/1.73 m2 in the elderly (67.18 ± 0.49 years). Among middle-aged people, eGFR was within G2 category (60–89 mL/min/1.73 m2) in 100 % of cases, while in 46 % of elderly individuals, it had decreased to G3a category (45–59 mL/min/1.73 m2). Normal or high eGFR (G1 category, ≥ 90 mL/min/1.73 m2) was preserved in only 10 % of elderly participants. Among middle-aged individuals with a slight decrease in eGFR within the G2 category (60–89 mL/min/1.73 m2), increased UACR was found in a third of the examined people, while in the elderly, a decrease in eGFR to 40–59 mL/min/1.73 m2 prevails, which is considered as chronic kidney disease within the G3a category accompanied by an increase in the UACR in 25 % of individuals. When assessing the functional state of the endothelium of large vessels, it was found that among the examined participants (n = 94) with different categories of eGFR (G1, G2, G3a), signs of endothelial dysfunction were observed in 54 (57.45 %).Of these, 19 patients (35.18 %) demonstrated severe impairment characterized by a vasospastic response to reactive hyperemia (by D.S. Celermajer method), indicating impaired endothelium-dependent vasodilation. Among individuals with endothelial dysfunction in large vessels, 70.4 % (n = 38) had UACR < 30 mg/g, 29.6 % (n = 16) had increased UACR: 10 people — at the level of 30–300 mg/g, and 6 people had UACR > 300 mg/g. At the same time, among individuals with preserved endothelial function, 65 % (n = 26) had UACR < 30 mg/g, 14 individuals had UACR of 30–300 mg/g, and none had UACR > 300 mg/g. Thus, UACR > 300 mg/g was recorded exclusively among patients with endothelial dysfunction (5 people, 9.2 %), showing a statistically significant difference (χ2 = 0.01; p = 0.03). Among individuals with eGFR reduced within categories G2 (60–89 mL/min/1.73 m2) and G3a (45–59 mL/min/1.73 m2), there was a decrease in microvascular endothelial function in 84 %. Among them, UACR < 30 mg/g was observed in 50.00 %, 30–300 mg/g — in 43.75 %, and > 300 mg/g — in 6.25 %. In participants with preserved microvascular endothelial function (16 %), the distribution was 33.3 % (< 30 mg/g) and 66.7 % (30–300 mg/g), with no individuals having UACR > 300 mg/g. Though this trend was not statistically significant (χ2 = 0.08, p = 0.13), it mirrored the association of UACR > 300 mg/g with large-vessel endothelial dysfunction. Importantly, a mutual burden phenomenon was observed in individuals with eGFR 45–89 mL/min/1.73 m2, with 56.25 % having combined large- and small-vessel endothelial dysfunction. Among them, 44.44 % had UACR of 30–300 mg/g and 11.11 % had UACR > 300 mg/g. The absence of UACR > 300 mg/g among patients with preserved endothelial function in both middle-aged and elderly groups confirms a strong association between significant albuminuria and endothelial dysfunction. UACR > 300 mg/g may indicate severe vascular wall damage and systemic endothelial dysfunction. To correct the detected changes, 39 individuals of various ages with manifestations of CRMS were prescribed Lespedeza capitata extract in addition to standard antihypertensive therapy. After one month of treatment, all patients showed an increase in flow-mediated dilation, indicating restored endothelial function in both large and microcirculatory vessels. Restoration of endothelial function was accompanied by a stable trend toward increased proportion of people with UACR < 30 mg/g (χ2 = 0.04, p = 0.07), suggesting improved kidney function with Lespedeza capitata extract. This effect is likely due to the proven nephroprotective action of Lespedeza capitata extract, making it a promising agent for the prevention and treatment of chronic kidney disease. Conclusions. Individuals of different age groups with CRMS demonstrated a mutual burden phenomenon: more than half of patients with eGFR of 45–89 mL/min/1.73 m2 (56.25 %) had both macro- and microvascular endothelial dysfunction, often accompanied by elevated UACR (> 300 mg/g in 11.11 %). These findings highlight the importance of UACR as a potential early marker of endothelial dysfunction during the initial stages of renal function decline. Elevated UACR may reflect existing endothelial injury, while low or moderate levels (UACR < 30 or 30–300 mg/g) may still be observed in patients with preserved endothelial function. For nephro- and angioprotection in individuals with CRMS, the addition of Lespedeza capitata extract to standard antihypertensive therapy is advisable.
кардіоренометаболічний синдром; хронічна хвороба нирок; функціональний стан ендотелію; Lespedeza capitata; ренопротекція; ангіопротекція
cardio-renal-metabolic syndrome; chronic kidney disease; endothelial function; Lespedeza capitata; nephroprotection; angioprotection