Журнал "Гастроэнтерология" 2 (56) 2015
Вернуться к номеру
Ингибиторы протонной помпы и риск межлекарственных взаимодействий
Авторы: Ткач С.М., Онищук Л.А. — Национальный медицинский университет имени А.А. Богомольца, г. Киев
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
В статье приведены современные данные о межлекарственных взаимодействиях ингибиторов протонной помпы (ИПП) с другими препаратами. Сделан вывод о том, что риск неблагоприятных межлекарственных взаимодействий усиливается при использовании ИПП и препаратов, преимущественно метаболизирующихся цитохромным изоферментом CYP2C19. При необходимости одновременного применения ИПП со многими другими препаратами, включая клопидогрель, предпочтение следует отдавать пантопразолу.
У статті наведені сучасні дані відносно міжлікарських взаємодій інгібіторів протонної помпи (ІПП) з іншими ліками. Зроблено висновок про те, що ризик несприятливих міжлікарських взаємодій підсилюється при застосуванні ІПП та препаратів, що переважно метаболізуються цито-хромним ізоферментом CYP2C19. За необхідності одночасного застосування ІПП з багатьма іншими ліками, включаючи клопідогрель, перевагу слід віддавати пантопразолу.
In the article, the current data regarding drug interactions of proton pomp inhibitors (PPI) with other preparations are discussed. It is concluded that the risk of adverse drug interactions is enhanced by the use of PPIs and drugs primarily metabolized by cytochrome isoenzyme CYP2C19. If the simultaneous application of IPP with many other drugs, including clopidogrel, is necessary, the preference should be given to pantoprazole.
ингибиторы протонной помпы, межлекарственные взаимодействия, система цитохрома Р450, пантопразол.
інгібітори протонної помпи, міжлікарські взаємодії, система Р450, пантопразол.
proton pomp inhibitors, drug interactions, cytochrome P450 system, pantoprazole.
Статья опубликована на с. 91-98
Введение
То, что многие лекарственные средства (ЛС) имеют токсический потенциал, который может причинять организму человека значительный вред, давно известно и общепризнано. Еще в 1870-х годах в некоторых странах Европы были сформированы специальные комитеты для исследования случаев потенциальной токсичности ЛС. Например, в 1870 году один из первых таких комитетов изучал случаи внезапной смерти, вызванной действием хлороформа. В 1922 году другой комитет изучал случаи желтухи у пациентов, которые принимали сальварсан. Знаковое исследование было проведено в 1937 году, когда в США сульфаниламид привел к смерти 107 человек [7]. После этого инцидента, а также многих других случаев зарегистрированной токсичности ЛС правительство США учредило Управление по контролю за продуктами питания и лекарственными средствами (Food and Drug Administration, FDA). Подобные организации сейчас существуют практически во всех странах мира.
Побочные реакции на ЛС являются ненамеренными вредными событиями, которые могут возникать при применении доз, используемых как для терапии, так и для профилактики любого состояния. Необходимо осознавать, что нет практически ни одного ЛС без потенциальной токсичности. Следовательно, все наши терапевтические вмешательства требуют взвешивания соотношения риска и пользы для каждого конкретного препарата. Особенно часто побочные реакции на ЛС встречаются у госпитализированных пациентов, которые обычно одновременно получают несколько препаратов. Так, один из метаанализов показал, что на 100 госпитализированных пациентов в среднем приходится 6,7 серьезной побочной реакции и 0,3 фатальной побочной реакции. Подсчитано, что побочные реакции на ЛС в США ежегодно приводят к смерти до 100 000 человек. Считается, что среди ведущих причин смерти побочные реакции на ЛС занимают 4–6-е место [7].
Перечень доступных современному практическому врачу средств для медикаментозного лечения желудочно-кишечных расстройств в последние годы резко расширился. Хотя многие новые препараты приводят к существенному и очень желаемому улучшению жизни пациентов, к сожалению, они имеют и негативную сторону — высокий потенциал серьезной токсичности. Такая токсичность основана как на естественном вредном для пациента потенциале новых препаратов, так и на постоянно возрастающей возможности нежелательных и потенциально опасных межлекарственных взаимодействий.
Межлекарственное взаимодействие лекарственных препаратов
Современный этап развития медицины характеризуется огромным прогрессом в фармакотерапии различных заболеваний, который привел к увеличению средней ожидаемой продолжительности жизни. Поскольку все больше и больше людей с хроническими заболеваниями доживают до преклонного возраста, существенно увеличивается и частота полифармации, то есть одновременного применения нескольких препаратов для лечения сочетанной патологии. Скорее всего, по мере дальнейшего старения населения полипрагмазия будет возрастать и в будущем. Исследования, проведенные в разных странах, свидетельствуют о том, что количество рецептов, которые выписываются пациентам, с возрастом увеличивается. Например, в США пациентам в возрасте свыше 80 лет в среднем выписывается 22 рецепта в год на более чем пять различных препаратов [12].
Следует сказать, что полифармация в клинической практике встречается достаточно часто, однако ее опасность практическими врачами недооценивается [24, 39]. Так, в возрасте 65 лет в среднем пациенты принимают 3–8 прописываемых и непрописываемых препаратов. Более 40 % пожилых пациентов принимают по меньшей мере одно лекарство, о котором не сообщают своему лечащему врачу [7]. Все это повышает вероятность возникновения нежелательных лекарственных взаимодействий, осуществляющихся системой CYP Р450. Так, если при совместном приеме 2 препаратов частота межлекарственных взаимодействий составляет 5 %, то при совместном приеме 5 препаратов они встречаются уже в каждом втором случае, а при совместном приеме 8 препаратов — наблюдаются всегда [24, 39, 40]. К препаратам, часто применяющимся в клинике и метаболизирующимся цитохромной системой, относятся ингибиторы протонной помпы (ИПП), диазепам, фенитоин, R-варфарин, бета-блокаторы, дигоксин, теофиллин, диклофенак, этанол, фенацетин, ацетаминофен, кларитромицин и многие другие [15, 16, 19].
Полифармация безусловно необходима, если у больного имеется сразу несколько серьезных заболеваний. Однако во многих случаях необходимости в полипрагмазии нет. Поэтому очень важно, чтобы думающие врачи всегда это осознавали и при возможности упрощали или рационализировали фармакотерапию у всех пациентов, особенно у пожилых людей, которые подвержены высокому риску возникновения побочных реакций на ЛС. Одним из наиболее важных видов медикаментозной токсичности является неблагоприятный результат взаимодействия нескольких лекарственных препаратов.
В практической гастроэнтерологии существует множество примеров неблагоприятного межлекарственного взаимодействия, которое может быть потенциально опасно для пациентов. Это касается многих гастроэнтерологических препаратов, включая ИПП, которые ввиду доказанной эффективности и безопасности считаются наиболее распространенными и популярными лекарственными средствами. Омепразол, лансопразол, пантопразол, рабепразол и эзомепразол используют в лечении нарушений, обусловленных действием соляной кислоты: гастроэзофагеальной рефлюксной болезни (ГЭРБ), пищевода Барретта, пептической язвенной болезни, функциональной диспепсии, синдрома Золлингера — Эллисона и других, более редких кислотозависимых заболеваний. Кроме того, ИПП являются обязательным компонентом эрадикационной терапии инфекции Helicobacter pylori и применяются для профилактики и лечения НПВП-гастропатий. В настоящее время ИПП стоят на первом месте среди 5 наиболее распространенных препаратов как по количеству потребителей, так и по общей стоимости (продажи ИПП превышают 10 миллиардов долларов США в год).
Ниже рассмотрены некоторые наиболее важные механизмы и случаи неблагоприятного межлекарственного взаимодействия на примере ИПП, которые относятся к одним из наиболее широко применяемых в мире ЛС (табл. 1) [15].
ИПП и препараты, требующие для всасывания кислой среды (итраконазол, кетоконазол, дигоксин). Пациенты, принимающие омепразол или другие ИПП, имеют риск снижения биологической усвояемости итраконазола и кетоконазола — имидазольных противогрибковых препаратов, применяемых при лечении серьезных диссеминированных грибковых инфекций, особенно у пациентов с иммунной недостаточностью, а также дигоксина — основного сердечного гликозида для лечения сердечной недостаточности и мерцательной аритмии. Такое взаимодействие препаратов является примером того, когда один препарат блокирует всасывание другого, что приводит к снижению уровня препарата в крови. Это происходит из-за того, что указанные препараты требуют кислой среды для всасывания [7].
ИПП и препараты, метаболизирующиеся системой CYP Р450. ИПП могут изменять метаболизм других препаратов путем индукции или ингибирования изоферментов цитохромной системы CYP Р450, таких как CYP2C19, 2D6 и 1A2, осуществляющих печеночный окислительный метаболизм многих ЛС [3, 6, 10–14]. Это особенно важно учитывать в случае с пациентами, которые одновременно с ИПП принимают препараты с узким терапевтическим окном, такие как диазепам, фенитоин и варфарин [15]. Феномен полиморфизма указанных ферментов Р450 имеет по крайне мере 2 клинически значимых эффекта. Во-первых, он может быть причиной генетически обусловленной индивидуальной вариабельности фармакологического эффекта некоторых препаратов, взаимодействующих с указанными энзимами. Во-вторых, если два или более препарата метаболизируются одним из этих ферментов, то это неизбежно приведет к их взаимодействию и, возможно, к взаимному антагонизму, что может вызвать повышение концентрации препарата в сыворотке крови, увеличить период его полураспада и в худшем случае — привести к побочным токсическим действиям [13].
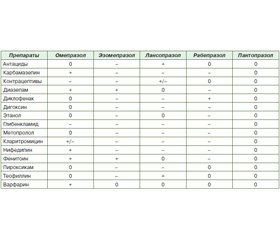
Установлено, что омепразол, эзомепразол и лансопразол обладают большим потенциалом нежелательных межлекарственных взаимодействий с такими группами препаратов, как антиконвульсанты, седативные препараты и миорелаксанты (например, фенитоин, мефенитоин, диазепам, флунитразепам, фенобарбитал, гексобарбитал, мефобарбитал и карисопродол). К еще более важным субстратам CYP2C19 относятся многие антидепрессанты (циталопрам, эсциталопрам, флуоксетин, сертралин, венлафаксин, имипрамин, кломипрамин, тримипрамин, амитриптилин, нортриптилин и моклобемид), а также некоторые другие лекарства, например пропранолол, варфарин, прогестерон, тестостерон и циклофосфамид [10–13, 16]. В отличие от омепразола, эзомепразола и лансопразола пантопразол демонстрирует существенно более низкий потенциал лекарственного взаимодействия, чем прочие ИПП, и наиболее хорошо изучен в этом отношении (табл. 2) [9, 15, 20, 24–26].
Клопидогрель и ИПП. В нескольких недавних исследованиях сообщалось о повышении кардиоваскулярной заболеваемости и смертности среди пациентов, одновременно принимающих клопидогрель и ИПП. Как известно, клопидогрель назначается после острого инфаркта миокарда или постановки коронарного стента, при этом очень часто для профилактики гастроинтестинального кровотечения назначаются и ИПП. Клопидогрель, как и ИПП, подвергается метаболизму в печени с участием изофермента CYP2C19 (CYP3A4) до своей активной формы [18, 37].
Антитромбоцитарный эффект клопидогреля разнится между пациентами. Так, пациенты с медленным метаболизмом препарата не могут эффективно преобразовывать клопидогрель в его активную форму, что приводит к пониженному антитромбоцитарному эффекту. В связи с этим в последнее время в фокусе интереса кардиологов и гастроэнтерологов оказались появившиеся сведения о негативном влиянии ИПП на антитромбоцитарное действие клопидогреля. Этот феномен, по-видимому, возникает по причине конкуренции между ИПП и клопидогрелем за один и тот же фермент CYP2C19. Генетические изменения в CYP2C19 связаны с более чем 50% повышением риска серьезных клинических исходов, включая смерть в результате сердечно-сосудистой патологии, инфаркта миокарда или инсульта, а также c троекратным повышением риска тромбоза стента у пациентов, получающих клопидогрель [13, 14, 18].
Обсервационные исследования и вторичные анализы данных клинических исследований по этому вопросу показали противоречивые результаты. Так, в исследовании среди 8205 ветеранов, госпитализированных по поводу острого коронарного синдрома, смерть вследствие повторной госпитализации была отмечена у 615 (20,8 %), получавших клопидогрель без ИПП, и у 1561 (29,8 %), получавшего клопидогрель в сочетании с ИПП, что повышало риск смерти или повторной госпитализации (добавочный относительный риск — 1,25). Другие исследования также подтвердили эти клинические наблюдения. Так, большое ретроспективное исследование стентированных пациентов, в течение 1 года получавших клопидогрель, показало большую частоту развития острого коронарного синдрома у 4521 больного, принимавшего клопидогрель и ИПП, чем у 9862 больных, принимавших клопидогрель как монотерапию (32,5 против 21,2 %). В другом ретроспективном исследовании Juurlink и соавт. показали, что среди 13 636 пациентов, которым клопидогрель назначался после выписки из больницы, где они находились по поводу острого инфаркта миокарда, дополнительное назначение ИПП в течение 30 дней ассоциировалось с повторными инфарктами (дополнительный относительный риск — 1,27) [2, 14, 25, 35, 38]. Было отмечено также, что только назначение пантопразола, который не ингибирует изофермент CYP2C19, не ассоциировалось с повторными инфарктами.
С другой стороны, в последнем двойном слепом клиническом исследовании COGENT с двойной имитацией фазы III «Клопидогрель и оптимизация клинических событий со стороны желудочно-кишечного тракта» («Clopidrogel and the Optimization of Gastrointestinal Events») были получены другие результаты. В этом исследовании пациенты с коронарными нарушениями получали двойную антитромбоцитарную терапию комбинацией аспирина и клопидогреля. Участники исследования были рандомизированы в группу приема ИПП (омепразол в дозе 20 мг) либо в группу приема плацебо. Было обследовано 3863 пациента, из которых 3627 пациентов были включены в исследование со средним сроком наблюдения 133 дня. У этих пациентов было зафиксировано 136 кардиоваскулярных (омепразол — 69; плацебо — 67; Р > 0,05) и 105 гастроинтестинальных (омепразол — 38; плацебо — 67; Р = 0,007) событий. Полученные данные показали, что применение омепразола в сочетании с клопидогрелем снижало риск развития желудочно-кишечного кровотечения по сравнению с комбинацией клопидогреля и плацебо и не приводило при этом к повышению риска осложнений со стороны сердечно-сосудистой системы. Таким образом, исследование COGENT не подтвердило гипотезу о том, что омепразол оказывает негативное влияние на антитромбоцитарную активность клопидогреля [20, 21]. Однако в письме от имени другой группы исследователей (Southworth и соавт.) относительно данного исследования говорилось, что клинические условия и конечные точки по сердечно-сосудистым явлениям, которые оценивались в исследовании COGENT, необходимо считать несостоятельными и ограничивающими возможность интерпретировать полученные данные [34]. Авторы письма предположили, что необходимо избегать совместного назначения клопидогреля и омепразола, о чем говорится в инструкции по применению клопидогреля.
Поэтому Управление по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) недвусмысленно указывает, что «FDA напоминает общественности о своем постоянном предупреждении о невозможности совместного применения препарата Plavix® (клопидогрель) и омепразола, поскольку такой комбинированный прием может вызвать значительное снижение уровней активных метаболитов клопидогреля и его антитромбоцитарной активности» [8]. Говоря о препаратах из группы ИПП, необходимо учесть, что данная рекомендация касается только омепразола, а не всех ИПП. Не все ИПП обладают одинаковым ингибирующим эффектом на изофермент CYP2C19, который играет решающую роль в преобразовании клопидогреля в его активную форму. В качестве альтернативного препарата из группы ИПП в данном случае следует рассматривать пантопразол. Это слабый ингибитор фермента CYP2C19, он оказывает менее существенный, чем омепразол, эффект на фармакологическую активность клопидогреля.
Учитывая противоречивость имеющихся на сегодняшний день данных, Американский колледж кардиологии, Американская кардиологическая ассоциация и Американский колледж гастроэнтерологии опубликовали заявление относительно совместного применения ИПП и клопидогреля. Суть этого заявления состоит в том, что, поскольку межлекарственные взаимодействия между ИПП и клопидогрелем пока не изучены на большом числе пациентов и не получены окончательные доказательства того, что применение ИПП снижает способность клопидогреля предупреждать коронарные синдромы, пациенты, получающие эти препараты, не должны менять свои медикаментозные режимы до тех пор, пока это специально не порекомендует их лечащий врач. Пациенты с наличием кислотозависимой патологии и высоким риском развития НПВП-гастропатий при необходимости приема НПВП или малых доз аспирина по-прежнему должны обязательно параллельно принимать ИПП [1, 4, 5].
Преимущества пантопразола при межлекарственных взаимодействиях ИПП. Важные клинические данные о потенциале лекарственных взаимодействий ИПП наиболее подробно изучены на примере омепразола и пантопразола. В частности, установлено, что омепразол и эзомепразол не только ингибируют свой собственный, опосредованный CYP2C19 метаболизм, но также могут влиять на особенности деградации других препаратов, метаболизм которых опосредован изоферментом CYP2C19 [3]. С клинической точки зрения одним из самых важных примеров лекарственного взаимодействия, индуцированного омепразолом, является снижение на (25 ± 50) % клиренса диазепама по причине конкурентного ингибирования CYP2C19 [6]. О возможном взаимодействии омепразола с другими бензодиазепинами, которые метаболизируются при участии системы цитохрома Р450, также необходимо помнить, в частности, это касается алпразолама, хлордиазепоксида, клоназепама и мидазолама. Поэтому пациентам, которые длительно получают терапию препаратами из группы бензодиазепинов, омепразол и эзомепразол назначать нельзя, в таких случаях препаратом выбора является пантопразол (в Украине недавно зарегистрирован новый пантопразол под торговой маркой Зованта®).
За исключением стандартных для ИПП взаимодействий с другими препаратами, которые связаны с повышением рН желудочного сока (взаимодействие с кетоконазолом, итраконазолом и дигоксином), в отношении пантопразола отмечены только единичные примеры лекарственного взаимодействия. В отличие от омепразола пантопразол (Зованта®) не вызывает взаимодействия при одновременном введении с фенитоином, варфарином, диазепамом, R-варфарином, бета-блокаторами, теофиллином, диклофенаком, фенацетином, ацетаминофеном, кларитромицином и другими препаратами, метаболизирующимися с участием CYP2C19 и CYP3A4 [24, 26]. Поэтому при необходимости длительного сочетанного применения ИПП и этих медикаментов он рассматривается как препарат выбора. В тех случаях, когда рекомендуется эрадикация инфекции H.pylori, наилучшим базисным препаратом также является пантопразол (Зованта®), который не вступает в конкурентные взаимоотношения с кларитромицином — основным антибиотиком в составе антихеликобактерной терапии, также метаболизирующимся цитохромной системой Р450 [10]. Такое сочетание снижает вероятность возникновения побочных эффектов и повышает эффективность лечения. Пантопразол также не вызывает клинически значимых перекрестных реакций с нестероидными противовоспалительными препаратами (НПВП), в первую очередь с диклофенаком, который является одним из наиболее часто применяемых препаратов этой группы [31, 35]. Поэтому при высоком риске возникновения НПВП-гастропатий, когда требуется дополнительное превентивное назначение ИПП, или при необходимости продолжения приема диклофенака даже в случае развития НПВП-гастропатии дополнительным лечебным препаратом выбора также является пантопразол (Зованта®).
Кроме того, пантопразол (Зованта®) также является наиболее безопасным ИПП и наилучшим по переносимости. При его приеме незначительные побочные эффекты фиксируются только у 1,1 % больных [8]. Программы контроля за результатами клинического применения показали, что среди 100 000 пациентов с кислотозависимыми расстройствами, получающих пантопразол, какие-либо неблагоприятные эффекты наблюдались только у 0,77 % [26, 30, 33]. Очень важно и то, что фармакокинетика пантопразола существенно не отличается у молодых и пожилых людей, которые являются основным контингентом пациентов, которым назначаются многочисленные препараты по поводу сопутствующей патологии. Кроме того, даже легкая и среднетяжелая дисфункция печени не влияет на фармакокинетику пантопразола, что обеспечивает стабильность его фармакологического эффекта [9, 33].
В отличие от других ИПП, которые обратимо связывают в протонной помпе или цистеин-813, или цистеин-321, пантопразол (Зованта®) связывается сразу с двумя цистеинами ПП — 813 и 822. Именно цистеин-822 обеспечивает устойчивость связи и длительность ингибиции протонной помпы и кислотной продукции. Поэтому если после прекращения приема других ИПП кислотность возвращается за счет прерывания химической связи с протонной помпой, то в случае с пантопразолом — за счет синтеза новых протонных помп, на который необходимо время. Поэтому и время для восстановления ингибированной секреции кислоты составляет для лансопразола около 15 часов, для омепразола и рабепразола — около 30 часов, в то время как для пантопразола — примерно 46 часов. То есть пантопразол (Зованта®) обеспечивает наиболее продолжительный кислотоснижающий эффект и является одним из наиболее эффективных и безопасных ИПП [9, 30, 32]. Хотя по конечному клиническому эффекту, особенно при пептических язвах, все ИПП примерно одинаковы, считается, однако, что в лечении язв желудка эффективность 4-недельного лечения пантопразолом достоверно выше, чем другими ИПП.
Заключение
Вопросы токсичности и непереносимости ЛС, а также неблагоприятных межлекарственных взаимодействий находятся в центре внимания регулирующих органов во всем мире. Наши основные надежды на решение этой проблемы в будущем связаны с дальнейшим развитием и внедрением в клиническую практику фармакогенетических исследований.
Опираясь на примеры, приведенные выше, можно сделать вывод, что существует два основных механизма взаимодействия препаратов. Первый представляет собой фармакокинетическое взаимодействие, при котором один препарат может менять концентрацию другого препарата в крови или в месте действия. Чаще всего такие взаимодействия препаратов происходят в результате конкурентного ингибирования ферментов, ответственных за метаболизм препарата. То есть когда совместно применяются два субстрата, метаболизирующиеся одним определенным ферментом, например каким-либо изоферментом цитохрома Р450, метаболизм препарата со сниженной аффинностью к этому изоферменту будет значительно замедлен, что приведет к снижению его выведения и повышению уровня в крови, если доза препарата не будет уменьшена. Как уже было сказано, в случае использования лекарств с узким терапевтическим окном, метаболизирующихся такими полиморфными изоферментами, как CYP2C19, 2D6 и 1A2, их генетически обусловленная сниженная активность у «медленных» и «промежуточных» метаболизаторов может приводить к повышению уровня препарата в крови, экстремальному изменению картины крови и неконтролируемым фармакологическим воздействиям. Этот механизм хорошо изучен и в настоящее время всегда учитывается в процессе разработки новых ЛС. В частности, многие фармацевтические компании крайне неохотно разрабатывают вещества, которые расщепляются с помощью изофермента CYP2D6, который обеспечивает распад большого числа высокоэффективных фармакологических субстанций в самых разных органах [40].
Второй механизм взаимодействия препаратов заключается в фармакодинамическом взаимодействии. При этом ни один взаимодействующий препарат не влияет на концентрацию другого, но их фармакологическое действие либо взаимно усиливается, либо уменьшается. Это взаимодействие менее распространено, чем фармакокинетическое, но клинически может быть очень серьезным.
Всестороннее понимание побочных эффектов ЛС крайне важно для практических врачей, поскольку лечение пациентов с применением постоянно появляющихся новых препаратов все время усложняется. Токсичность лекарственных препаратов в гастроэнтерологии и гепатологии остается существенной проблемой, которая, по всей видимости, будет усугубляться, поскольку продолжительность жизни пациентов увеличивается и они все чаще лечатся с применением большого количества препаратов. Возникновение значительного количества побочных эффектов ЛС можно объяснить нежелательным взаимодействием препаратов.
1. Abraham N.S., Hlatky M.A., Antman E.M. et al. ACCF/ACG/AHA-2010 expert consensus document on the concomitant use of proton pump inhibitors and thienopyridines: a focused update of the ACCF/ACG/AHA-2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use. A report of the American college of cardiology foundation task force on expert consensus documents // J. Am. Coll. Cardiol. — 2010. — 56 (24). — 2051–2066.
2. Banerjee S., Weideman R.A., Weideman M.W. et al. Effect of concomitant use of clopidogrel and proton pump inhibitors after percutaneous coronary intervention // Am. J. Cardiol. — 2011. — 107. — 871–878.
3. Bekkers C.H., Touw D.J., Lamers C.B., Geus W.P. The effect of CYP2C19 polymorphism on the pharmacokinetics and acid-inhibitory effects of oral lansoprazole and omeprazole // Br. J. Clin. Pharmacol. — 2002. — 54 (5). — 553.
4. Bhatt D.L., Cryer B.L., Contant C.F. et al. Clopidogrel with or without omeprazole in coronary artery disease // N. Engl. J. Med. — 2010. — 363 (20). — 1909–1917.
5. Bhatt D.L., Scheiman J., Abraham N.S. et al. ACCF/ACG/AHA-2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use // Am. J. Gastroenterol. — 2008. — 103. — 2890–2907.
6. Desta Z., Zhao X., Shin J.G., Flockhart D.A. Clinical significance of the cytochrome P450 2C19 genetic polymorphism // Clin. Pharmacokinet. — 2002. — 41. — 913–958.
7. Egan L.J. Mechanisms of Drug Toxicity or Intolerance // Dig. Dis. — 2011. — 29. — 172–176
8. FDA reminder to avoid concomitant use of Plavix (clopidogrel) and omeprazole. — www.fda.gov/Drugs/DrugSafety/ucm231161. htm
9. Fitton A., Wiseman L. Pantoprazole. A review of its pharmacological properties and therapeutic use in acid–related disorders // Drugs. — 1996. — 51 (3). — 460–482.
10. Furuta T., Shirai N., Sugimoto M., Nakamura A., Hishida A., Ishizaki T. Influence of CYP2C19 pharmacogenetic polymorphism on proton pump inhibitor-based therapies // Drug Metab. Pharmacokinet. — 2005. — 20 (3). — 53–167.
11. Furuta T., Sugimoto M., Shirai N., Ishizaki T. CYP2C19 pharmacogenomics associated with therapy of Helicobacter pylori infection and gastro-esophageal reflux diseases with a proton pump inhibitor // Pharmacogenomics. — 2007. — 8. — 1199–1210.
12. Gardiner S.J., Begg E.J. Pharmacogenetics, drug-metabolizing enzymes, and clinical practice // Pharmacol. Rev. — 2006. — 58 (3). — 521–590.
13. Gerson L.B., Triadafilopoulos G. Proton pump inhibitors and their drug interactions: an evidence-based approach // Eur. J. Gastroenterol. Hepatol. — 2001. — 13 (5). — 611–616.
14. Gilard M., Arnaud B., Cornily J.C. et al. Influence of omeprazole on the antiplatelet action of clopidogrel associated with aspirin: the randomized, double-blind OCLA (Omeprazole Clopidogrel Aspirin) study // J. Am. Coll. Cardiol. — 2008. — 51. — 256–260.
15. Hagymási K., Müllner K., Herszényi L., Tulassay Z. Update on the pharmacogenomics of proton pump inhibitors // Pharmacogenomics. — 2011. — 12 (6). — 873–888.
16. Hunfeld N.G., Mathot R.A., Touw D.J., van Schaik R.H., Mulder P.G., Franck P.F., Kuipers E.J., Geus W.P. Effect of CYP2C19*2 and *17 mutations on pharmacodynamics and kinetics of proton pump inhibitors in Caucasians // Br. J. Clin. Pharmacol. — 2008. — 65. — 752–760.
17. Johnson D.A. Concomitant use of PPIs and antiplatelet therapy // Gastroenterol. Hepatol. — 2011. — 7. — 7–10.
18. Juhasz M., Herszenyi L., Tulassay Z.S. Current standings of the proton pump inhibitor and clopidrogel co–therapy: review on an evolving field with the eyes of the gastroenterologist // Digestion. — 2010. — 81 (1). — 10–15.
19. Kazui M., Nishiya Y., Ishizuka T. et al. Identification of the human cytochrome P450 enzymes involved in the two oxidative steps in the bioactivation of clopidogrel to its pharmacologically active metabolite // Drug Metab. Dispos. — 2010. — 38. — 92–99.
20. Kromer W. Similarities and Differences in the Properties of Substituted Benzimidazoles: A Comparison detween Pantoprazole and Related Compounds // Digestion. — 1995. — 56. — 443–454.
21. Kwok C.S., Jeevanantham V., Dawn B. et al. No consistent evidence of differential cardiovascular risk amongst proton-pump inhibitors when used with clopidogrel: meta-analysis // Int. J. Cardiol. — 2012 Mar 29. Epub ahead of print.
22. Kwok C.S., Loke Y.K. Effects of proton pump inhibitors on platelet function in patients receiving clopidogrel: a systematic review // Drug Saf. — 2012. — 35. — 127–139.
23. Laine L., Hennekens C. Proton pump inhibitor and clopidrogel interaction: fact or fiction? // Am. J. Gastroenterol. — 2010. — 105 (1). — 34–41.
24. Lee K.C., Ma J.D., Kuo G.M. Pharmacogenomics: bridging the gap between science and practice // J. Am. Pharm. Assoc. — 2010. — 50 (1). — e1–e17.
25. Li X.-Q., Andersson T.B., Ahlstrom M., Weidolf L. Comparison of inhibitory effects of the proton pump-inhibiting drugs omeprazole, esomeprazole, lansoprazole, pantoprazole, and rabeprazole on human cytochrome P450 activities // Drug Metab. Dis. — 2004. — 32 (8). — 821–827.
26. Mullin J.M., Gabello M., Murray L.J. et al. Proton pump inhbitors: actions and reactions // Drug Disc. Today. — 2009. — 14 (13–14). — 647–660.
27. Ogawa R., Echizen H. Drug-drug interaction profiles of proton pump inhibitors // Clin. Pharmacokinet. — 2010. — 49 (8). — 509–533.
28. Ray W.A., Murray K.T., Griffin M.R. et al. Outcomes with concurrent use of clopidogrel and proton-pump inhibitors: a cohort study // Ann. Intern. Med. — 2010. — 152. — 337–345.
29. Robinson M., Horn J. Clinical pharmacology of proton pump inhibitors: what the practising physician needs to know // Drugs. — 2003. — 63 (24). — 2739–2754.
30. Sachs G., Shin J. Differential reversal of inhibition of gastric H/K-ATPase following pantoprazole or omeprazole administration // Am. J. Gzstroenterol. — 2001. — 96. — S71.Abstr.223
31. Sakai T., Aoyama N., Kita T. et al. CYP2C19 genotype and pharmacokinetics of three proton pump inhibitors in healthy subjects // Pharm. Res. — 2001. — 18 (6). — 721–727.
32. Shin J.M., Sachs G. Pharmacology of proton pump inhibitors // Curr. Gastroenterol. Rep. — 2008. — 10 (6). — 528–534.
33. Steinijans V., Huber R., Hartmann M. et al. Lack of pantoprazole drug interactions in man: an updated review // Int. J. Clin. Pharmacol. Ther. — 1996. — 34 (1 Suppl.). — S31–S50.
34. Southworth M.R., Temple R. Interaction of clopidogrel and omeprazole // N. Engl. J. Med. — 2010. — 363 (20). — 1977.
35. Tanaka M., Ohkubo T., Otani K. et al. Stereoselective pharmacokinetics of pantoprazole, a proton pump inhibitor, in extensive and poor metabolizers of S-mephenytoin // Clin. Pharmacol. Ther. — 2001. — 69 (3). — 108–113.
36. Trifiro G., Corrao S., Alacqua M. et al. Interaction risk with proton pump inhibitors in general practice: significant disagreement between different drug-related information sources // Br. J. Clin. Pharmacol. — 2006. — 62 (5). — 582–590.
37. Tucker G. The interaction of proton pump inhibitors with the cytochromes P450 // Aliment. Pharmacol. Ther. — 1994. — 8. — 33–38
38. Van Boxel O.S., van Oijen M.G., Hagenaars M.P. et al. Cardiovascular and gastrointestinal outcomes in clopidogrel users on proton pump inhibitors: results of a large Dutch cohort study // Am. J. Gastroenterol. — 2010. — 105. — 2430–2436. — quiz, 2437.
39. Volpe M., Chin D., Paneni F. The challenge of polypharmacy in cardiovascular medicine // Fundam. Clin. Pharmacol. — 2010. — 24. — 9–17.
40. Zanger U.M., Turpeinen M., Klein K., Scwab M. Functional pharmacogenetics/genomics of human cytochromes P450 involved in drug biotransformation // Anal. Bioanal. Chem. — 2008. — 392 (6). — 1093–1108.

/93/93.jpg)
/94/94.jpg)