Международный неврологический журнал 4 (66) 2014
Вернуться к номеру
Нейротрофическая терапия депрессий: возможности и перспективы
Авторы: Марута Н.А., Явдак И.А., Череднякова Е.С., Марута О.С. - ГУ «Институт неврологии, психиатрии и наркологии НАМН Украины», г. Харьков
Рубрики: Неврология, Психиатрия
Разделы: Клинические исследования
Версия для печати
С целью оценки эффективности применения пpeпapaтa Церебролизин в комплексном лечении депрессивных и когнитивных расстройств у больных дисциркуляторной энцефалопатией II стадии, обусловленной атеросклерозом, проведено комплексное клиническое и нейропсихологическое обследование (оценка когнитивной продуктивности по краткой шкале оценки психического статуса (MMSE); умственной работоспособности и утомляемости по таблице Крепелина; памяти по методике заучивания десяти слов (по А.Р. Лурия); депрессивного состояния по шкале MADRS; уровня личностной и реактивной (ситуационной) тревожности по методу Спилбергера — Ханина; качества жизни с помощью опросника EuroQol EQ-5D) 60 пациентов с диагнозом «депрессивное расстройство органического (сосудистого) генеза». Показано позитивное влияние нейротрофической терапии в виде внутривенного введения Церебролизина на редукцию депрессивной симптоматики, улучшение когнитивных функций и качества жизни больных дисциркуляторной энцефалопатией ІІ стадии сосудистого (атеросклеротического) генеза. Применение Церебролизина в комплексной терапии депрессии при дисциркуляторной энцефалопатии способствует повышению эффективности терапии, что подтверждается регрессом анергического компонента депрессии и когнитивных расстройств (внимания, памяти) и во многом объясняется участием нейротрофических механизмов в генезе сосудистых депрессивных расстройств.
З метою оцінки ефективності застосування пpeпapaту Церебролізин у комплексному лікуванні депресивних і когнітивних розладів у хворих на дисциркуляторну енцефалопатію II стадії, обумовлену атеросклерозом, проведено комплексне клінічне і нейропсихологічне обстеження (оцінка когнітивної продуктивності за короткою шкалою оцінки психічного статусу (MMSE); розумової працездатності та стомлюваності за таблицею Крепеліна; пам’яті за методикою заучування десяти слів (по А.Р. Лурія); депресивного стану за шкалою MADRS; рівня особової і реактивної (ситуаційної) тривожності за методом Спілбергера — Ханіна; якості життя за допомогою питальника EuroQol EQ-5D) 60 пацієнтів з діагнозом «депресивний розлад органічного (судинного) генезу». Показано позитивний вплив нейротрофічної терапії у вигляді внутрішньовенного введення Церебролізину на редукцію депресивної симптоматики, поліпшення когнітивних функцій і якості життя хворих на дисциркуляторну енцефалопатію ІІ стадії судинного (атеросклеротичного) генезу. Застосування Церебролізину в комплексній терапії депресії при дисциркуляторній енцефалопатії сприяє підвищенню ефективності терапії, що підтверджується регресом анергічного компонента депресії і когнітивних розладів (уваги, пам’яті) і багато в чому пояснюється участю нейротрофічних механізмів у генезі судинних депресивних розладів.
In order to assess the effectiveness of Cerebrolysin in comprehensive treatment of depression and cognitive impairment in patients with dyscirculatory encephalopathy stage II due to atherosclerosis we have conducted a comprehensive clinical and neuropsychological evaluation (assessment of cognitive efficiency on Mini-mental state examination scale (MMSE); mental performance and fatigue on Kraepelin’s table; memory method of learning ten words (by A.R. Luria); depressive state by MADRS scale; level of personal and reactive (situational) anxiety by Spielberger — Khanin method; quality of life using a questionnaire EuroQol EQ-5D of 60 patients with diagnosis «depressive disorder of organic (vascular) origin». It was shown a positive impact of neurotrophic therapy in the form of intravenous Cerebrolysin introduction on the reduction of depressive symptoms, improvement of cognitive functions and quality of life of patients with dyscirculatory encephalopathy stage II of vascular (atherosclerotic) origin. Application of Cerebrolysin in the complex therapy of depression in dyscirculatory encephalopathy enhances the effectiveness of therapy, as evidenced by regression of anergic depression component and cognitive disorders (of attention, memory) and is largely due to the participation of neurotrophic mechanisms in the origin of vascular depression.
депрессии, когнитивные расстройства, нейротрофическая терапия, Церебролизин.
депресії, когнітивні розлади, нейротрофічна терапія, Церебролізин.
depression, cognitive disorders, neurotrophic therapy, Cerebrolysin.
Статья опубликована на с. 70-79
Высокая распространенность и выраженность медико-социальных последствий депрессий в виде хронизации, рецидивирования, резистентности, нарушений социального функционирования, качества жизни и суицидального поведения возводят проблему в ранг наиболее актуальных, требующих изучения в плане ранней диагностики и оптимизации терапии психозов [1–7].
Одной из наиболее важных причин, обусловливающих столь значительные медико-социальные последствия депрессий, является их коморбидность в широком смысле слова, когда депрессии не только протекают сочетанно с различными формами патологии, но и становятся факторами риска и ухудшения исхода для других форм патологии.
В проведенных исследованиях показано, что депрессия повышает риск развития таких заболеваний, как ишемический инсульт (в 1,8 раза), болезнь Альцгеймера (в 2,1 раза), ишемическая болезнь сердца (в 1,5 раза) и др. [8].
Также установлено, что присоединившаяся депрессия ухудшает прогноз соматических и неврологических заболеваний, повышая показатели смертности, тяжести заболевания и развития осложнений.
В связи с этим важными представляются данные о том, что при кардиоваскулярных заболеваниях депрессия повышает смертность в 3,5-4 раза и ухудшает исход заболевания; при инсульте показатели смертности возрастают в 3,4 раза и существенно задерживается функциональное восстановление; при эпилепсии нарастает тяжесть заболевания и нарушается социальное функционирование [8].
Особо неблагоприятные медико-социальные последствия характерны для депрессивных расстройств, которые развиваются при цереброваскулярной патологии [9–13]. Указанные расстройства соответствуют рубрике МКБ-10 «Депрессивное расстройство органической природы» (F 06.32), развиваются у лиц старше 45 лет и характеризуются сложными коморбидными взаимоотношениями сосудистой и аффективной патологии, результатом чего является анергия, выраженный когнитивный дефицит и прогрессирующее нарушение социального функционирования.
В последнее время активно исследуется возможность эффективной терапии депрессивных расстройств в пожилом возрасте на наиболее ранних стадиях цереброваскулярных заболеваний [14–16]. Исходя из современных представлений о патогенезе депрессивных расстройств, которые развиваются при дисциркуляторной энцефалопатии (ДЭ), весьма перспективным представляется применение препаратов, улучшающих метаболизм мозговой ткани и обладающих нейропротективными свойствами. Одним из препаратов, обладающих выраженным метаболическим действием, является Церебролизин, клиническая эффективность и мультимодальное нейроспецифическое действие которого были установлены в различных экспериментальных исследованиях. Также его клиническая эффективность подтверждена в ходе проспективных рандомизированных двойных слепых плацебо-контролируемых клинических исследований [17–20].
С целью оценки эффективности применения пpeпapaтa Церебролизин в комплексном лечении депрессивных и когнитивных расстройств у больных ДЭ II стадии, обусловленной атеросклерозом, проведено исследование 60 пациентов обоих полов в возрасте от 45 до 65 лет (средний возраст — 56,63 ± 6,32 года у больных основной группы и 57,43 ± 5,48 — у больных контрольной группы) с диагнозом «депрессивное расстройство органического (сосудистого) генеза» в соответствии с критериями МКБ-10, находящихся на амбулаторном лечении в ГУ «Институт неврологии, психиатрии и наркологии НАМН Украины».
Диагноз ДЭ II стадии атеросклеротического генеза устанавливался на основании жалоб больных, данных анамнеза, неврологического, психиатрического статусов и подтверждался результатами инструментальных (магнитно-резонансная томография головного мозга, ультразвуковая допплерография экстра- и интракраниальных сосудов, офтальмоскопия) и лабораторных (концентрация в крови b-липопротеидов) методов обследования.
В исследование включались пациенты, давшие письменное информированное согласие на участие в исследовании и соответствующие критериям включения/исключения.
Все пациенты случайным образом были распределены в основную (30 человек) и контрольную (30 человек) группы лечения. Пациенты основной группы получали дополнительно к базовой терапии (витаминотерапия, вазоактивные средства, антидепрессанты) Церебролизин по 10 мл в/в (всего по 15 вливаний на 21-дневный курс терапии), пациенты контрольной группы получали базовую терапию без использования Церебролизина.
Продолжительность лечения и исследования для каждого пациента составила 3 недели (21 день).
Все больные проходили комплексное клиническое (с оценкой соматического, неврологического и психопатологического состояния) и нейропсихологическое обследование (исследование когнитивной продуктивности по краткой шкале оценки психического статуса (Mini-Mental State Examination, MMSE) [21]; исследование умственной работоспособности и утомляемости по таблице Крепелина [22]; исследование памяти по методике заучивания десяти слов (по А.Р. Лурия) [23]; оценка депрессивного состояния по шкале MADRS (Montgomery-Asberg Depression Rating Scale) [24]; оценка уровня личностной и реактивной (ситуационной) тревожности по методу Спилбергера — Ханина [25]; исследование качества жизни с помощью опросника Европейской группы качества жизни (EuroQol EQ-5D) [26]) до и после курсового лечения.
Исходное состояние вошедших в исследование пациентов оценивалось по данным объективного обследования на основе регистрации жалоб больных, данных неврологического и психического состояния.
В неврологическом статусе до лечения наиболее часто встречались цефалгический (93,3 % больных основной и 96,7 % больных контрольной группы), вестибуло-атактический (63,3 % больных основной и 60,0 % больных контрольной группы), подкорковый (33,3 % больных основной и 40,0 % больных контрольной группы) синдромы, синдром артериальной гипертензии (46,7 % больных основной и 53,3 % больных контрольной группы), экстрапирамидная недостаточность (30,0 % больных основной и 36,7 % больных контрольной группы) и сенсорные расстройства (30,0 % больных основной и 23,3 % больных контрольной группы).
В структуре психопатологических проявлений у всех обследуемых доминировали депрессивная симптоматика и когнитивные расстройства.
Депрессивная симптоматика проявлялась преимущественно сниженным настроением, апатией, снижением интересов и чувств, энергичности, нарушениями сна, снижением аппетита и сочеталась с тревогой разной степени интенсивности (76,67 % больных основной и 73,33 % больных контрольной группы) и ипохондрическими переживаниями (43,33 % больных основной и 46,67 % больных контрольной группы). На основании особенностей клинических проявлений у обследованных были выделены следующие типы депрессии: апатическая (40,00 % больных основной и 43,33 % больных контрольной группы), астеническая (43,33 % больных основной и 36,67 % больных контрольной группы), ипохондрическая (16,67 % больных основной и 20,00 % больных контрольной группы).
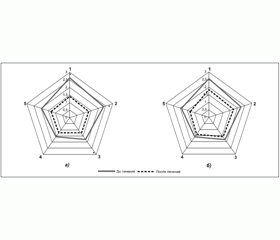
Профили диаграмм, отражающие субъективные жалобы больных до и после проведенного лечения, представлены на рис. 1.
Согласно приведенным данным, до начала терапии субъективные жалобы больных сравниваемых групп были идентичны как по представленности, так и по степени выраженности.
Наибольшую интенсивность имели такие симптомы, как снижение работоспособности (2,08 и 2,02 балла у больных основной и контрольной групп соответственно), слабость (1,98 и 1,92 балла у больных основной и контрольной групп соответственно), подавленность (1,92 и 1,88 балла у больных основной и контрольной групп соответственно), рассеянное внимание (1,88 и 1,94 баллов у больных основной и контрольной групп соответственно), снижение памяти (1,86 и 1,84 балла у больных основной и контрольной групп соответственно), апатия (1,86 и 1,82 балла у больных основной и контрольной групп соответственно).
После проведенного лечения более выраженная позитивная динамика у больных основной группы отмечена по всем оцениваемым симптомам, особенно в оценке снижения памяти (0,88 балла у больных основной группы в сравнении с 1,32 балла у больных группы контроля), рассеянного внимания (0,92 балла у больных основной группы в сравнении с 1,16 балла у больных группы контроля), слабости (0,96 балла у больных основной группы в сравнении с 1,22 балла у больных группы контроля), снижения работоспособности (1,14 балла у больных основной группы в сравнении с 1,38 балла у больных группы контроля), подавленности (0,76 балла у больных основной группы в сравнении с 1,08 балла у больных группы контроля), апатии (0,72 балла у больных основной группы в сравнении с 0,96 балла у больных группы контроля).
Динамика состояния больных по выделенным типам депрессии в процессе лечения представлена на рис. 2.
/72/72_2.jpg)
Согласно приведенным на рис. 2 данным, после 21-дневного курса лечения больных с оценкой «без перемен», а также «выздоровление» не было.
Рассматривая динамику депрессивного состояния по типам депрессии в основной группе, мы установили, что достоверно лучшая динамика выявлена у больных с астеническим (преобладание категории «значительное улучшение» наряду с «улучшением») и апатическим (равнозначное распределение «улучшения» и «значительного улучшения») типами депрессии.
У большинства больных основной группы с ипохондрическим типом депрессии динамика состояния соответствовала умеренной, существенных различий при данном типе депрессии между группами не установлено.
У больных контрольной группы динамика состояния по всем типам депрессии распределилась по категориям «незначительное улучшение», «улучшение» и «значительное улучшение». При этом для большей части больных, независимо от типа депрессии, было характерно «улучшение».
Полученные данные демонстрируют достоверно лучшую динамику редукции депрессивного состояния у больных основной группы, преимущественно при астеническом и апатическом типах депрессии.
Таким образом, по окончании трехнедельного курса лечения отмечался статистически значимый регресс большинства клинических симптомов (депрессивного, когнитивного и астенического спектра).
Тестирование пациентов по краткой шкале оценки психического статуса (MMSE) позволило оценить когнитивную продуктивность. Полученные данные представлены в табл. 1 и графически — на рис. 3, 4.
Согласно приведенным данным, до начала лечения степень нарушений когнитивной продуктивности по шкале MMSE у больных сравниваемых групп была идентичной и в среднем по группам соответствовала деменции легкой степени выраженности (21,77 и 21,90 балла у больных основной и контрольной групп соответственно).
Полученные данные демонстрируют, что до начала лечения у всех пациентов обеих групп наблюдались нарушения когнитивных функций разной степени выраженности. При этом не было выявлено пациентов с расстройствами, соответствующими рубрикам «Тяжелая деменция» (0–10 баллов) и «Когнитивная продуктивность не нарушена» (28–30 баллов).
На момент включения в исследование деменция умеренной степени выраженности (11–19 баллов) установлена у одинакового количества больных сравниваемых групп — по 8 (26,67 %) обследованных. У 13 (43,33 %) пациентов основной группы и 12 (40,00 %) — контрольной группы показатели соответствовали деменции легкой степени выраженности (20–23 балла), у 9 (30,00 %) пациентов основной группы и 10 (33,33 %) пациентов контрольной группы выраженность нарушений когнитивной продуктивности по шкале MMSE свидетельствовали о преддементных нарушениях (24–27 баллов).
Как видно из данных, приведенных в табл. 1, на 21-й день лечения в обеих группах больных ДЭ II стадии сосудистого генеза произошли позитивные изменения показателей когнитивной продуктивности. Вместе с тем изменения у больных основной группы отражали достоверно более значимую положительную динамику.
Так, деменция умеренной степени выраженности (11–19 баллов) по окончании курса лечения установлена лишь у 2 (6,67 %) больных основной группы (против 5 (16,67 %) больных группы контроля).
Деменция легкой степени выраженности (20–23 балла) имела место у 7 (23,33 %) больных основной группы и у 10 (33,33 %) больных контрольной группы.
После завершения терапии количество больных с преддементными нарушениями (24–27 баллов) не имело статистических различий в группах сравнения (14 (46,67 %) и 13 (43,33 %) соответственно), тогда как в основной группе обследованных без признаков нарушения когнитивной продуктивности (28–30 баллов) было достоверно больше (7 (23,33 %) против 2 (6,67 %) в группе контроля).
То есть под влиянием терапии в основной группе увеличилось число больных с преддементными нарушениями (46,67 %) и без нарушений когнитивной продуктивности (23,33 %), тогда как большинство больных группы контроля, несмотря на улучшение состояния, находилось в диапазоне деменции легкой степени выраженности (33,33 %) и преддементных нарушений (43,33 %). Достоверные различия между группами после 21-дневного лечения установлены в категориях «Деменция легкой степени выраженности» (достоверно меньше среди больных основной группы) и «Когнитивная продуктивность не нарушена» (достоверно больше среди больных основной группы).
По завершении лечения степень нарушений когнитивной продуктивности по шкале MMSE у больных сравниваемых групп имела достоверные различия (средний балл в основной группе — 25,10, в группе контроля — 23,23). При этом средние показатели в основной группе соответствовали преддементным нарушениям (24–27 баллов), а в группе контроля — деменции легкой степени выраженности (20–23 балла).
Таким образом, выявленные между сравниваемыми группами значимые различия в показателях когнитивной продуктивности по шкале MMSE демонстрируют большую эффективность терапии у больных основной группы.
Анализ динамики умственной работоспособности с помощью таблиц Крепелина показал, что до начала лечения у больных ДЭ ІІ степени сосудистого генеза обеих групп наблюдалось постепенное снижение темпа умственной деятельности в ходе выполнения задания (рис. 5) и наличие низких показателей работоспособности (табл. 2), что свидетельствовало о выраженной истощаемости произвольного внимания данных пациентов.
Данные, полученные через 21 день терапии, демонстрируют позитивную динамику у больных обеих групп: наблюдается возрастание продуктивности и устойчивости внимания. При этом у пациентов основной группы под влиянием лечения отмечалось более выраженное возрастание продуктивности внимания (рис. 4) и коэффициента работоспособности (до 0,83 при р ≤ 0,05) по сравнению с пациентами контрольной группы, где данный показатель составил 0,68. Такая динамика свидетельствует о существенном улучшении функций произвольного внимания и повышении работоспособности у пациентов с ДЭ ІІ степени сосудистого генеза после проведенного курса лечения с дополнительным применением Церебролизина.
Оценка состояния кратковременной памяти исследуемых больных в динамике лечения проводилась с помощью методики заучивания десяти слов (по А.Р. Лурия). Общее количество воспроизведенных слов после каждого предъявления до и после проведенного лечения представлено на рис. 6.
Как свидетельствуют представленные на рисунке 6 данные, до начала лечения у больных ДЭ ІІ степени сосудистого генеза наблюдалось снижение показателей объема памяти и отсутствие стойкого увеличения количества правильно воспроизведенных слов. Кривая запоминания характеризовалась зигзагообразной формой, что свидетельствовало о неустойчивости и высокой истощаемости мнестических процессов.
Исследование объема кратковременной памяти через 21 день терапии продемонстрировало возрастание показателей мнестических функций у пациентов обеих групп, отмечалось постепенное нарастание объема кратковременной памяти (рис. 6, табл. 3).
При этом у пациентов, получавших в качестве дополнительной терапии Церебролизин, отмечалось более значимое улучшение функций кратковременной памяти: уже при первом предъявлении стимульного материала после проведенного лечения объем кратковременной памяти обследованных составил 7,23, в то время как у пациентов контрольной группы — 6,38 (при р ≤ 0,05), а максимальное количество воспроизведенных слов у большинства пациентов основной группы отмечалось уже на 5-й пробе, тогда как у пациентов контрольной группы объем кратковременной памяти достигал своего максимума лишь на 6–7-м предъявлении.
Следовательно, данные проведенного исследования демонстрируют значительное улучшение познавательных функций, в частности памяти и внимания, у больных ДЭ ІІ степени сосудистого генеза при дополнительном включении в терапию Церебролизина.
Оценка психического состояния больных проводилась с помощью клинико-психопатологического метода и психометрических тестов (шкала MADRS) для оценки депрессивного состояния и метода Спилбергера — Ханина для оценки уровня личностной и реактивной (ситуационной) тревожности.
До начала лечения суммарный балл по шкале MADRS у больных исследуемых групп был идентичным и находился в диапазоне от 27 до 30 баллов, что соответствовало умеренной депрессии (средний балл в основной группе — 28,2, в контрольной — 27,8). В процессе лечения депрессивная симптоматика прогредиентно уменьшалась: средний показатель шкалы МАDRS на 21-й день лечения в основной группе составил 18,2 балла, в контрольной — 21,4 балла, что соответствовало уменьшению симптомов депрессии до легкой степени у больных обеих групп. Вместе с тем динамика регресса депрессивной симптоматики у больных основной группы была более выраженной.
Рассматривая динамику показателей MADRS по отдельным пунктам (рис. 7), следует отметить, что у больных основной группы уменьшение показателей по пунктам «Трудности концентрации», «Вялость», «Наблюдаемая печаль» и «Печаль, о которой пациент говорит» опережало таковое у больных контрольной группы и через 3 недели терапии показатели снизились достоверно больше, что свидетельствовало о лучшем ответе на лечение у данной категории больных.
/76/76.jpg)
Отсутствия изменений в показателях депрессии по шкале МАDRS под влиянием 21-дневной терапии в сравниваемых группах выявлено не было, что согласуется с динамикой показателей субъективных жалоб больных основной и контрольной групп.
Динамика распределения больных ДЭ ІІ cтепени сосудистого генеза по уровню тревожности по шкале Спилбергера — Ханина под влиянием терапии представлена в табл. 4.
Согласно представленным данным, до начала лечения у пациентов обеих групп имела место тревожность разной степени выраженности. Большая часть больных характеризовались низкой степенью тревожности (30–39 баллов) — по 18 (60,00 %) в каждой из групп. Высокая степень тревожности (40–49 баллов) была зарегистрирована у 5 (16,67 %) больных основной группы и у 4 (13,33 %) больных контрольной группы, отсутствие тревожности (20–29 баллов) зарегистрировано у 7 (23,33 %) больных основной группы и 8 (26,67 %) больных группы контроля.
В процессе 21–дневного лечения наблюдалась положительная динамика показателей тревожности в группах сравнения (табл. 4).
В основной группе после проведенного лечения отсутствие тревожности зарегистрировано у 18 (60,0 %) больных, в контрольной группе — у 16 (53,3 %) больных. Низкая степень тревожности после лечения отмечалась у 12 (40,0 %) больных основной и у 14 (46,67 %) больных контрольной группы. Высокая степень тревожности по завершении исследования не была зарегистрирована ни у кого из обследованных.
Приведенные данные показывают, что после проведенного курса 21-дневной терапии показатели тревожности достоверно снизились у больных обеих групп. При этом статистически значимых различий в динамике показателей тревожности между сравниваемыми группами выявлено не было.
Исследование качества жизни больных ДЭ ІІ cтепени сосудистого генеза обеих групп до и после 21-дневного лечения проводилось с помощью опросника Европейской группы качества жизни (EuroQol EQ–5D).
Данные по группам, полученные до и после лечения при оценке пяти компонентов, связанных с такими аспектами жизни, как подвижность, самообслуживание, активность в повседневной жизни, боль/дискомфорт и беспокойство/депрессия, представлены графически в виде профиля состояния здоровья на рис. 8.
Согласно представленным данным, до начала лечения показатели по всем пяти компонентам в группах сравнения были идентичны.
Данные, полученные после проведенного 21-дневного лечения, демонстрируют наличие различий в показателях между сравниваемыми группами по всем компонентам опросника Европейской группы качества жизни: больные основной группы характеризовались более высокими оценками состояния собственного здоровья, особенно по шкалам «беспокойство/депрессия», «активность в повседневной жизни», «подвижность».
Использование при работе с опросником EuroQol EQ–5D визуально–аналоговой шкалы (так называемого «термометра здоровья») позволило получить количественную оценку общего статуса здоровья больных и выявить динамику в самооценке больными состояния собственного здоровья в процессе терапии. Так, до лечения средние показатели в сравниваемых группах были сопоставимы и не имели достоверных различий (32 — у больных основной группы и 35 — у больных группы контроля), тогда как после проведенной терапии у больных основной группы наблюдалось достоверно более выраженное увеличение среднего показателя самооценки общего состояния их здоровья (84 — у больных основной группы и 62 — у больных контрольной группы).
Результаты опросника EuroQol EQ-5D свидетельствуют, что в группе больных, принимавших дополнительно к терапии Церебролизин, прирост доли пациентов с восстановлением активности в повседневной жизни, подвижности, способности к самообслуживанию на фоне уменьшения депрессивных и болевых проявлений был более значительным, чем в группе контроля.
Таким образом, проведенное исследование продемонстрировало позитивное влияние нейротрофической терапии в виде внутривенного введения Церебролизина на редукцию депрессивной симптоматики, улучшение когнитивных функций и качества жизни больных ДЭ ІІ степени сосудистого (атеросклеротического) генеза.
Применение Церебролизина в комплексной терапии депрессии при ДЭ способствует повышению эффективности терапии, что подтверждается регрессом анергического компонента депрессии и когнитивных расстройств (внимание, память) и во многом объясняется участием нейротрофических механизмов в генезе сосудистых депрессивных расстройств.
1. Вознесенская Т.Г. Депрессия в пожилом возрасте // Cons. Med. — 2009. — 11 (2). — 74–79.
2. Марута Н.О., Панько Т.В., Череднякова О.С. Клініко-психопатологічні особливості депресій у осіб похилого віку / Міжнародний психіатричний, психотерапевтичний та психоаналітичний журнал. — 2008. — Т. 2, № 1, 2 (2, 3). — С. 24–27.
3. Марута Н.А., Явдак И.А. Особенности формирования аутоагрессии у больных депрессивным эпизодом пожилого возраста // Український вісник психоневрології. — 2010. — Т. 18, вип. 3(64). — С. 136–137
4. Alexopoulos G.S., Murphy C.F., Gunning-Dixon F.M. et al. Microstructural white matter abnormalities and remission of geriatric depression // Am. J. Psychiatry. — 2008. — 165. — 238–244.
5. Chen H. Trophic factors counteract elevated FGF-2-induced inhibition of adult neurogenesis // Neurobiol of aging. — 2007. — 28(8). — 1148–62.
6. Lorenzetti V., Allen N.B., Fornito A. еt al. Structural brain abnormalities in major depressive disorder: A selective review of recent MRI studies // J. Affective Disorders. — 2009. — 117. — 1–17.
7. Taqui A.M., Itrat A., Qidwai W., Qadri Z. Depression in the elderly: does family system play a role? A cross-sectional study // BMC Psychiat. — 2007. — 7. — 7–57.
8. Schaffer Al., McIntosh D., Goldstein B.I., Rector N.A., McIntyre R.S., Beaulieu S., Swinson R., Yatham L.N. The CANMAT task force recommendations for the management of patients with mood disorders and comorbid anxiety disorders // Canadian Network for Mood and Anxiety Treatments (CANMAT) Task Force. — 2012. — 24(1). — 6–22.
9. Зозуля Ю.П., Міщенко Т.С. Проблеми судинно–церебральної патології та шляхи їх вирішення // Журн. НАМН України. — 2011. — Т. 17, № 1. — С. 19–25.
10. Круглов Л.С., Мешандин И.А. Оптимизация терапии пожилых больных с коморбидностью депрессии и психоорганических нарушений сосудистого генеза // Психиатрия и психофармакотерапия. — 2012. — Т. 14, № 2. — С. 40–45.
11. Мешандин И.А. Динамика клинических характеристик и социального функционирования в процессе терапии больных позднего возраста с сочетанием депрессивного расстройства и психоорганических нарушений сосудистого генеза: Автореферат дис... канд. мед. наук. — СПб., 2012. — 194 с.
12. Aarsland D., Pahlhagen S., Ballard C.G., Svenningsson U.E. & P. Depression in Parkinson disease — epidemiology, mechanisms and management // Nat. Rev. Neurol. — 2012. — 8. — 35–47.
13. Alexopoulos G.S. The vascular depression hypothesis: 10 years later // Biological Psychiatry. — 2006. — 60. — 1304–1305.
14. Марута Н.А. Возможности антидепрессивной терапии в ХХІ веке // Нейроnews-Киев. — 2008. — № 6 (11). — С. 24–28.
15. Мосолов С.Н. Биологические механизмы развития рекуррентной депрессии и действия антидепрессантов: новые данные // Психофармакотерапия депрессий. — 2011. — 15. — 1–14.
16. Кожина А.М., Гайчук Л.М. Терапевтические подходы к коррекции депрессивных расстройств // Психічне здоров’я. — 2007. — № 3(16). — С. 67–68.
17. Пантелеева Г.П., Артюх В.В., Крылова Е.С. и др. Оптимизация психофармакотерапии эндогенных депрессий с помощью препарата Церебролизин // Психиатрия и психофармакотерапия. — 2012. — № 1.
18. Дамулин И.В., Коберская Н.Н., Мхитрян Э.А. Влияние церебролизина на умеренные когнитивные расстройства // Журн. неврологии и психиатрии. — 2007. — 2. — 86–89.
19. Суслина З.А., Максимова М.Ю., Федорова Т.Н. Оксидантный стресс и основные направления нейропротекции при нарушениях мозгового кровообращения // Неврологический журнал. — 2007. — № 4. — С. 4–8.
20. Чуканова Е.И. Церебролизин в лечении пациентов с синдромом мягкого когнитивного снижения // Трудный пациент. — 2008. — 6 (2–3). — 3–6.
21. Практикум по общей, экспериментальной и прикладной психологии / Под ред. А.А. Крылова, С.А. Маничева. — 2-е изд. — СПб.: Питер, 2003. — 560 с.
22. Оценка умственной работоспособности по Э. Крепелину // Елисеев О.П. Практикум по психологии личности. — СПб., 2003. — С. 199–200.
23. Лурия А.Р. Основы нейропсихологии. — М.: Academia, 2003.
24. Montgomery S.A., Asberg M. A new depression scale designed to be sensitive to change // British Journal of Psychiatry. — 1979. — 134 (4). — 382–389.
25. Исследование тревожности (Ч.Д. Спилбергер, адаптация Ю.Л. Ханин) // Диагностика эмоционально-нравственного развития / Ред. и сост. И.Б. Дерманова. — СПб., 2002. — С. 124–126.
26. Новик Н.А., Ионова Т.Н. Руководство по исследованию качества жизни в медицине. — М: ОЛМА-ПРЕСС, 2002. — 320 c.

/72/72.jpg)
/73/73.jpg)
/74/74.jpg)
/75/75.jpg)
/75/75_2.jpg)
/77/77.jpg)
/77/77_2.jpg)