Журнал «Почки» 2 (04) 2013
Вернуться к номеру
Тромботична тромбоцитопенічна мікроангіопатія
Авторы: Таран О.І. - Кафедра нефрології та нирково-замісної терапії НМАПО імені П.Л. Шупика, м. Київ
Рубрики: Нефрология
Разделы: Медицинское образование
Версия для печати
Визначення поняття
Тромботична тромбоцитопенічна мікроангіопатія (ТМА) — судинне ураження (переважно артеріол і капілярів) різних органів унаслідок ушкодження ендотелію та оклюзія просвіту судин тромбоцитарними тромбами. Існує декілька форм ТМА, що наведені в табл. 1.
Усім формам ТМА притаманні загальні риси: утворення тромбів у капілярах, артеріолах, артеріях, а відмінності — в типі органів, які вражаються: ГУС — судини нирок; ТТП — судини головного мозку та інших органів (у тому числі нирок).
Етіологія
ТМА розвивається на тлі інфекційних захворювань, що викликані: I. E-coli; Shigella dystyntria (вживання недовареного м’яса, непастеризованого молока, немитих фруктів, овочів, некип’яченої води). II. Пневмококом. III. ВІЛ.
Патогенез
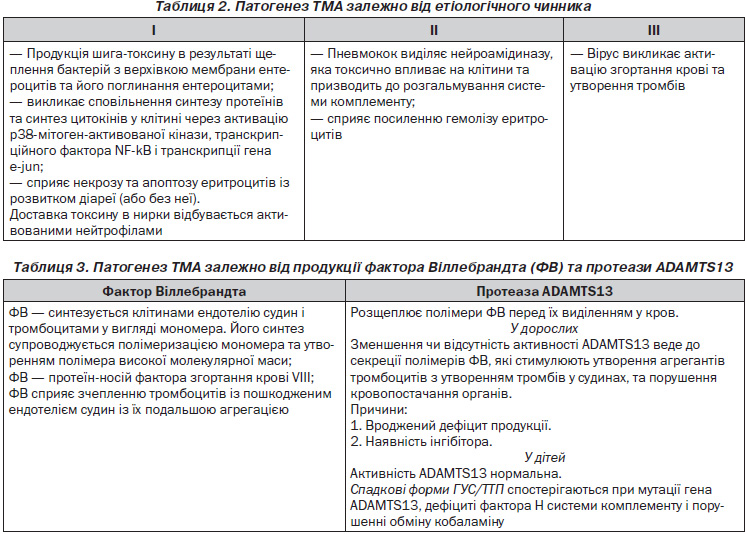
Патогенетичний розвиток ТМА залежить від етіологічного чинника та деяких факторів згортання крові й агрегації тромбоцитів, вплив яких наведений у табл. 2, 3.
Присутність у циркуляції великих мультимерів ФВ — важливий механізм агрегації тромбоцитів та швидкого утворення тромбів.
ТМА — системні захворювання, що включають ряд хвороб, які не є типовими запальними хворобами або васкулітами. За даними Роберта В. Шрайєра (2009), такі системні захворювання, як ССД, ТТП, ГУС, злоякісна АГ, АФС, хоча і проявляються гематурією, сечовим синдромом та АГ, однак гістологічно відрізняються від змін, що спостерігаються при гломерулонефриті (ГН).
Загальні гістологічні зміни:
— тромбоз капілярів клубочків та аферентних артеріол, ушкодження ендотелію з фібриноїдним некрозом;
— при АГ та ССД буває субінтимальна проліферація;
— імунофлюоресцентні та електронно-мікроскопічні зміни не показові.
Клінічна симптоматика ГУС (Д+)
У хворих спостерігається слабкість та загальмованість, різка блідість шкіри, іноді — жовтяниця або пурпура. Відмічається невелика лихоманка, абдомінальний біль, нудота, блювота. Розвивається кривава діарея в середньому протягом 7 днів.
Ураження центральної нервової система (ЦНС):
— судоми, сонливість, порушення зору, афазія, сплутаність свідомості, кома (50 % хворих).
Ураження серця:
— за сукупністю факторів (анемія, гіпергідратація, підвищення артеріального тиску (АТ)) розвивається серцево-судинна недостатність.
Ураження шлунково-кишкового тракту (ШКТ):
— інфаркти або перфорація кишкової стінки;
— кишкова непрохідність;
— гепатоспленомегалія — 20–40 % хворих;
— у 20 % розвиток цукрового діабету (ЦД), у тяжких випадках — інфаркт підшлункової залози;
— рідко вражаються легені, очі, м’язи (рабдоміоліз).
Ураження нирок:
— олігурія протягом 7–10 днів;
— у 50 % хворих виникає гостре ураження нирок (ГУН), або помірне зниження швидкості клубочкової фільтрації (ШКФ), або без порушення функції нирок;
— помірно або незначно підвищений АТ;
— зазвичай — сечовий синдром та мікрогематурія, рідше — значна макрогематурія та масивна протеїнурія;
— дегідратація внаслідок діареї (гіповолемічний шок) або гіпергідратація внаслідок анурії.
Клінічна симптоматика ГУС (Д–) (атиповий)
Захворювання часто розпочинається після респіраторної вірусної інфекції. Однаково часто хворіють як підлітки, так і дорослі.
Ураження нирок:
— ГУН розвивається у 50 % пацієнтів, у цих же хворих можливий перехід у хронічну ниркову недостатність (ХНН);
— розвивається тяжка або злоякісна АГ.
Ураження центральної нервової системи:
— енцефалопатія, у дорослих — геморагічні інсульти.
Ураження ШКТ:
— нудота, блювота, біль у животі. Кривава діарея не характерна.
Клінічна симптоматика ТТП
Захворювання може бути як єдиним епізодом після вдалого лікування, так і перебігати з рецидивами. Розпочинається частіше після грипоподібного синдрому. У дебюті хвороби визначається висока лихоманка, спостерігаються різної локалізації кровотечі (шлунково-кишкові, носові, маткові) поєднано зі шкірною пурпурою.
Ураження нирок:
— сечовий синдром із помірною протеїнурією та мікрогематурією. Рідко спостерігається макрогематурія та утворення еритроцитарних циліндрів; олігурія розвивається рідко;
— спостерігається тяжка АГ;
— у 40–80 % пацієнтів визначається порушення функції нирок;
— у 25 % пацієнтів фіксується зниження ШКФ менше 40 мл/хв через рік від початку захворювання.
Ураження ЦНС:
— тяжка енцефалопатія (нестійка, зникає через 2 доби), нерідко — з вогнищевими нефрологічними симптомами;
— у 10 % пацієнтів може розвинутись мозкова кома.
Ураження серця:
— інфаркти міокарда виникають у 15 % пацієнтів;
— спостерігаються порушення ритму та провідності;
— гостра серцево-судинна недостатність може виникати у 10 % хворих;
— іноді у хворих настає раптова смерть.
Спостерігаються ураження легенів, підшлункової залози, наднирникових залоз.
Клінічна симптоматика ГУС/ТТП унаслідок інфекції пневмококом:
— частота виникнення захворювання нижча, ніж після інших інфекцій. Розвитку хвороби передують пневмонія, менінгіт або сепсис. За перебігом ця клінічна форма ТМА більш тяжка, ніж ТМА іншої етіології. У структурі ГУС/ТТП без діареї займає 40 %;
— анемія, тромбоцитопенія, олігурія та ГУН;
— показники згортання крові в нормі при відсутності ДВЗ-синдрому;
— смертність — у 25 % випадків;
— розвиток ХНН частіший, ніж при іншій етіології.
Клінічна симптоматика ГУС/ТТП унаслідок дефіциту фактора Н комплементу:
— спадковий тип, але при генеалогічному аналізі прояви цієї хвороби можуть бути відсутніми у родичів;
— перебіг тяжкий із рецидивами;
— за клінічними даними схожий на нетипову форму;
— у пацієнта знижені концентрації С3- та Н-фракції комплементу;
— у капілярах клубочків є включення комплементу та спостерігається проліферація мезангію;
— прогноз у цілому несприятливий;
— перспективна трансплантація нирок і печінки одночасно, оскільки печінка виробляє фактори комплементу.
Клінічна симптоматика ГУС/ТТП унаслідок дефіциту ензиму ADAMTS13:
— маніфестує з народженням або протягом перших років життя;
— гемолітична анемія, жовтяниця, тромбоцитопенія;
— сечовий синдром, АГ, ХНН;
— можуть уражуватись інші органи, що і зумовлює клінічну симптоматику.
Клінічна симптоматика ТТП, асоційована з вагітністю, — гостра ТТП, HELLP-синдром, післяпологовий ГУС (чи відрізняється від ТТП без вагітності — невідомо):
— Гостра ТТП розвивається в 24–28 тижнів, за симптоматикою нагадує прееклампсію.
— HELLP-синдром у 70 % випадків розвивається в допологовому періоді або через 24–28 годин після пологів, особливо при неускладненій вагітності (Мухін О.М. і співавт., 2006). За даними Р.В. Шрайера (2009) — частіше в ІІІ триместрі і дуже рідко — в перші дні вагітності.
Клінічна симптоматика: тяжка прееклампсія: АГ, ураження нирок, печінки. Розвиваються гемолітична анемія, тромбоцитопенія. Перебіг може ускладнитись розвитком ГУН, рідше — поліорганною недостатністю та ДВЗ-синдромом (25 %). Ускладнюється також відшаруванням плаценти та внутрішньоутробною асфіксією.
— Післяпологовий ГУС може розвинутись через 6 місяців після нормальних пологів.
Діагностика
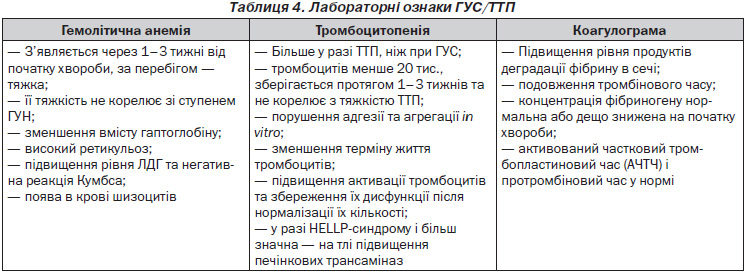
При підозрі на розвиток ТМА виконуються такі лабораторні (загальний аналіз крові, маркери гемолізу (ретикулоцити, лактатдегідрогеназа (ЛДГ)); біохімічний аналіз крові; вміст сечової кислоти, коагулограма та визначення функції тромбоцитів; реакція Кумбса; загальний аналіз разової та добової сечі; визначення ШКФ; загальний аналіз калу та його бактеріологічний аналіз) та інструментальні (ультразвукова діагностика органів черевної порожнини; біопсія нирки (тільки у разі ТТП та атипових ГУС для диференціальної діагностики зі швидкопрогресуючим ГН) методи дослідження. Лабораторні показники деяких аналізів крові наведені в табл. 4.
Лейкоцитоз розвивається при типовому ГУС, може спостерігатися зсув лейкоцитарної формули вліво. Вираженість ступеня зрушення формули корелює з прогнозом хвороби. У хворих визначається також гіперурикемія.
Лабораторними ознаками HELLP-синдрому є підвищення вмісту ЛДГ понад 600 МО/л та відсотка фрагментованих еритроцитів у циркулюючій крові (гемоліз) на тлі значної тромбоцитопенії (менше 100 • 109/л). Спостерігається значне підвищення вмісту печінкових трансаміназ.
Лікування
Етіопатогенетичне лікування ТМА залежить від її клінічної форми. Типовий ГУС передбачає проведення симптоматичної терапії на тлі дієти з обмеженням вживання харчового білка та застосування інгібіторів АПФ у дозах, відповідних ШКФ, та з урахуванням рівня АТ.
Хворим корегують об’єм циркулюючої крові та в подальшому підтримують колоїдно-осмотичний тиск крові. Дітям призначають високі дози вітаміну Е — 1 г/м2/добу протягом одного тижня. У разі необхідности проводять гемодіаліз. При кровотечах призначають введення свіжих еритроцитів і тромбоцитів. Не призначають антибактеріальних препаратів та дезагрегантів.
Пневмококовий ГУС/ТТП. Хворим переливають свіжезаморожену плазму (СЗП) на тлі плазмаферезу або без такого, щоденно або через день до нормалізації кількості тромбоцитів у крові. Для профілактики рецидиву ГУС/ТТП призначають низькі дози аспірину та дипіридамолу.
ГУС/ТТП унаслідок дефіциту ADAMTS13 або Н-фракції комплементу. Лікування полягає в призначенні СЗП по 10–20 мл/кг/добу на тлі плазмаферезу. Якщо є можливість визначити вміст ADAMTS13 та її інгібіторів і виявляється їх велика кількість, то розпочинають хіміотерапію або видаляють селезінку.
ГУС/ТТП. Основним методом лікування є введення безцитратної плазми (БЦП). Інфузії БЦП викликають припинення внутрішньосудинного тромбоутворення за рахунок компонентів плазми. БЦП уводять в/в крапельно по 30–40 мл/кг/добу — 1 добу; 10–20 мл/кг/добу — до нормалізації ЛДГ, кількості тромбоцитів та розвитку ремісії. Поєднане лікування інфузіями БЦП та плазмаферезом є більш ефективним, особливо у разі ГУН. Необхідно видаляти один об’єм плазми за сеанс (40 мл/кг) із її заміщенням адекватною кількістю БЦП.
Інфузії БЦП можуть використовуватись для підтримуючої терапії.
ТМА, асоційована з вагітністю. Лікування полягає у введенні БЦП до розвитку повної ремісії. Переривання вагітності проводять тільки при неефективності БЦП. У разі розвитку HELLP-синдрому вагітність переривається і проводиться симптоматична терапія.

1. Нефрология: Национальное руководство (глав. ред. — акад. РАМН Н.А. Мухин). — М.: ГЭОТАР-Медиа, 2009. — С. 345-359.
2. Рациональная фармакотерапия в нефрологии: Руководство для практикующих врачей / Под ред. Н.А. Мухина, А.В. Козловской, Е.М. Шилова. — М.: Литтерра, 2006. — С. 388-399.
3. Руководство по нефрологии / Под ред. Роберта В. Шрайера: Перевод с анг. — М.: ГЭОТАР-Медиа. — 2009. — С. 303-394, 418.