Журнал «Боль. Суставы. Позвоночник» Том 12, №2, 2022
Вернуться к номеру
Антиостеопоротичне лікування та ризик COVID-19: чи існує зв’язок?
Авторы: Григор’єва Н.В., Бистрицька М.А., Заверуха Н.В., Мусієнко А.С.
ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України», м. Київ, Україна
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Актуальність. Незважаючи на нещодавні рекомендації ASBMR, AACE, Endocrine Society, ECTS&NOF щодо лікування остеопорозу в епоху COVID-19, вплив антиостеопоротичних препаратів на ризик і тяжкість захворювання вивчений недостатньо. Метою дослідження було оцінити ризик COVID-19 у хворих з остеопорозом, які отримують парентеральне лікування бісфосфонатами або деносумабом, а також тяжкість його перебігу у вищезазначеного контингенту. Матеріали та методи. Ми провели телефонне опитування та проаналізували дані 195 пацієнтів (92 % жінок; середній вік 62,7 ± 10,8 року) із системним остеопорозом залежно від поточного застосування парентеральних антирезорбтивних препаратів (золедронова кислота, ібандронова кислота або деносумаб, n = 125) і порівняли результати з даними хворих з остеопорозом, які раніше не застосовували жодних антиостеопоротичних препаратів (n = 70). Результати. Серед обстежених на COVID-19 захворіли 32,9 % осіб, які не отримували будь-якого антиостеопоротичного лікування в минулому, та 33,3 % хворих з остеопорозом, які отримували лікування парентеральними резорбентами (p > 0,05). Серед осіб, які приймали золедронову кислоту, захворіли 29,2 %, ібандронову кислоту — 34,4 %, деносумаб — 42,9 %. Вірогідних відмінностей у частоті та тяжкості COVID-19 залежно від наявності та типу антиостеопоротичної терапії не було виявлено. Крім того, не встановлено відмінностей показників залежно від віку пацієнтів, їх статі, наявності ожиріння та інших факторів ризику остеопорозу. Ризик COVID-19 у пацієнтів із системним остеопорозом не відрізнявся залежно від застосування антирезорбтивних препаратів: відношення шансів (OR) становило 1,1 (95% ДІ 0,6–2,0), або від застосування певного антиостеопоротичного препарату (для золедронової кислоти — 0,9 (95% ДІ 0,4–2,0), ібандронової кислоти — 1,1 (95% ДІ 0,5–2,3) та для деносумабу — 1,6 (95% ДІ 0,5–5,2). Висновки. Парентеральні антиостеопоротичні препарати (золедронова або ібандронова кислоти, деносумаб) не впливають на частоту та тяжкість COVID-19 і можуть бути рекомендовані для продовження лікування хворих на остеопороз під час COVID-19.
Introduction. Despite the recent ASBMR, AACE, Endocrine Society, ECTS&NOF guidelines for osteoporosis management in the era of COVID-19 the impact of antiosteoporotic drugs on disease risk and severity is insufficiently studied. The purpose of this study was to assess the COVID-19 risk for the patients receiving the parenteral bisphosphonate or Denosumab treatment, and the severity of its course in patients with systemic osteoporosis. Materials and methods. We performed the phone survey and studied the results of 195 patients (92 % women; mean age – 62.7 ± 10.8 years) with systemic osteoporosis depending on the current use of parenteral antiresorptive drugs (Zoledronic, Ibandronic acids, or Denosumab, n = 125) and compared the results with data of the patients with osteoporosis who did not use any anti-osteoporotic drugs previously (n = 70). Results. The group of patients with COVID-19 included 32.9 % of patients who did not receive previously any anti-osteoporotic treatment and 33.3 % of osteoporotic patients treated with parenteral antiresorptive drugs. The share of the patients taking the Zoledronic acid who fell ill with COVID-19 was 29.2 %, the share of those taking the Ibandronic acid was 34.4 %, and the share of those taking Denosumab was 42.9 %. We did not reveal any significant differences in the COVID-19 frequency and severity depending on the presence and type of parenteral anti-osteoporotic therapy. Additionally, there were no differences depending on the patients' age, gender, obesity, and other osteoporosis risk factors. The risk of COVID-19 in the patients with systemic osteoporosis did not differ depending on antiresorptive drug use, amounting (odds ratio (OR) 95 % CI) 1.1 (0.6-2.0), or on the use of the definite anti-osteoporotic drug (for the Zoledronic acid – 0.9 (0.4-2.0), the Ibandronic acid – 1.1 (0.5-2.3), and for the Denosumab – 1.6 (0.5-5.2). Conclusions. Parenteral anti-osteoporotic drugs (Zoledronic acid, Ibandronic acid, or Denosumab) do not have any influence on COVID-19 frequency and severity and can be recommended for the continuation of the treatment of patients with osteoporosis.
COVID-19; антирезорбтивні препарати; остеопороз; золедронова кислота; ібандронова кислота; деносумаб
COVID-19; antiresorptive drugs; osteoporosis; Zoledronic acid; Ibandronic acid; Denosumab
Вступ
Матеріали та методи
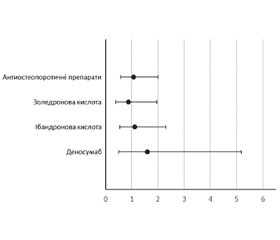
Результати
/12.jpg)
Обговорення
Висновки
- World Health Organization. Weekly epidemiological update on COVID-19. Режим доступу: https://www.who.int/emergencies/diseases/novel-coronavirus-2019/situation-reports.
- Офіційний інформаційний портал Міністерства охорони здоров’я України. Коронавірус в Україні. Режим доступу: https://covid19.gov.ua.
- Johns Hopkins Coronavirus Resource Center. COVID-19 dashboard by the Center for Systems Science and Engineering at Johns Hopkins University [Internet]. Johns Hopkins Coronavirus Resource Center. 2022. Режим доступу: https://coronavirus.jhu.edu.
- Fuggle N.R., Singer A., Gill C. et al. Correction to: How has COVID-19 affected the treatment of osteoporosis? An IOF-NOF-ESCEO global survey. Osteoporos. Int. 2021. 32(4). 611-617. doi: 10.1007/s00198-021-05905-7. PMID: 33751152; PMCID: PMC7942214.
- Blanch-Rubió J., Soldevila-Domenech N., Tío L. et al., Group TCS. Influence of anti-osteoporosis treatments on the incidence of COVID-19 in patients with non-inflammatory rheumatic conditions. Aging (Albany, NY). 2020. 12(20). 19923-19937. doi: 10.18632/aging.104117. PMID: 33080571; PMCID: PMC7655189.
- Formenti A.M., Pedone E., di Filippo L., Ulivieri F.M., Giustina A. Are women with osteoporosis treated with denosumab at risk of severe COVID-19? Endocrine. 2020. 70(2). 203-205. doi: 10.1007/s12020-020-02500-4. PMID: 32951069; PMCID: PMC7502215.
- Yu E.W., Tsourdi E., Clarke B.L., Bauer D.C., Drake M.T. Osteoporosis management in the era of COVID-19. J. Bone Miner. Res. 2020. 35(6). 1009-1013. doi: 10.1002/jbmr.4049. PMID: 32406536; PMCID: PMC7273005.
- Girgis C.M., Clifton-Bligh R.J. Osteoporosis in the age of COVID-19. Osteoporos. Int. 2020. 31(7). 1189-1191. doi: 10.1007/s00198-020-05413-0. PMID: 32346775; PMCID: PMC7187664.
- Napoli N., Elderkin A.L., Kiel D.P., Khosla S. Managing fragility fractures during the COVID-19 pandemic. Nat. Rev. Endocrinol. 2020. 16(9). 467-468. doi: 10.1038/s41574-020-0379-z. PMID: 32528045; PMCID: PMC7288256.
- Joint Guidance on Osteoporosis Management in the Era of COVID-19 from the ASBMR, AACE, Endocrine Society, ECTS & NOF. Режим доступу: https://www.asbmr.org/about/statement-detail/joint-guidance-on-osteoporosis-management-covid-19.
- Salvio G., Gianfelice C., Firmani F. et al. Remote management of osteoporosis in the first wave of the COVID-19 pandemic. Arch. Osteoporos. 2022. 17(1). 37. doi: 10.1007/s11657-022-01069-x. PMID: 35235056; PMCID: PMC8889057.
- Smadja D.M., Mentzer S.J., Fontenay M. et al. COVID-19 is a systemic vascular hemopathy: insight for mechanistic and clinical aspects. Angiogenesis. 2021. 24(4). 755-788. doi: 10.1007/s10456-021-09805-6. PMID: 34184164; PMCID: PMC8238037.
- Smetana K. Jr., Rosel D., Brábek J. Raloxifene and Bazedoxifene Could Be Promising Candidates for Preventing the COVID-19 Related Cytokine Storm, ARDS and Mortality. In Vivo. 2020. 34(5). 3027-3028. doi: 10.21873/invivo.12135. PMID: 32871847; PMCID: PMC7652447.
- Hampson G., Stone M., Lindsay J.R., Crowley R.K., Ralston S.H. Diagnosis and Management of Osteoporosis During COVID-19: Systematic Review and Practical Guidance. Calcif. Tissue Int. 2021. 109(4). 351-362. doi: 10.1007/s00223-021-00858-9. PMID: 34003337; PMCID: PMC8129963.
- Huang C.F., Shiao M.S., Mao T.Y. Retrospective Analysis of the Effects of Non-Compliance with Denosumab on Changes in Bone Mineral Density During the COVID-19 Pandemic. Patient Prefer Adherence. 2021. 15. 1579-1584. doi: 10.2147/PPA.S316144. PMID: 34290494; PMCID: PMC8289459.

/12_2.jpg)