Статья опубликована на с. 105-112
Методология
Методы, использованные для сбора/селекции доказательств: поиск в электронной базе данных.
Описание методов, использованных для сбора/селекции доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрайновскую библиотеку, базы данных EMBASE и MEDLINE. Глубина поиска составляла 7 лет.
Методы, использованные для оценки качества и силы доказательств:
— консенсус экспертов;
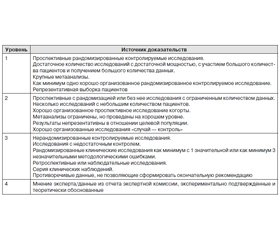
— оценка значимости в соответствии с уровнями доказательности и классами рекомендаций (прилагаются).
Методы, использованные для анализа доказательств:
— обзоры опубликованных метаанализов;
— систематические обзоры с таблицами доказательств.
Описание методов, использованных для анализа доказательств
Были использованы:
— Сахарный диабет. Острые и хронические осложнения / Под ред. И.И. Дедова, М.В. Шестаковой. — М., 2011. — 477 с.;
— Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под ред. И.И. Дедова, М.В. Шестаковой. — М., 2013. — Вып. 6;
— International consensus on the Management and Prevention on the Diabetic Foot, International working group on the Diabetic foot, 2011;
— World Union of Wound Healing Societies (WUWHS) «Principles of best practice: Wound exudate and 5 the role of dressings». A consensus document. — London: MEP Ltd., 2007;
— World Union of Wound Healing Societies (WUWHS). Minimising pain at wound dressing-related procedures. A consensus document. — Toronto, Ontario, Canada: Wound Pedia Inc., 2007;
— Diabetes, Pre-Diabetes and Cardiovascular Diseases EASD and ESC Guideline, 2013.
Методы, использованные для формулирования рекомендаций:
— консенсус экспертов.
Индикаторы доброкачественной практики (Good Practice Points — GPPs):
— рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций, конфликт интересов отсутствует.
Экономический анализ
Анализ стоимости не проводился, и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
— внешняя экспертная оценка;
— внутренняя экспертная оценка.
Описание метода валидизации рекомендаций
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего то, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей-эндокринологов и врачей-хирургов первичного звена в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался, и вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультации и экспертная оценка
Проект рекомендаций был рецензирован также независимыми экспертами, которых попросили прокомментировать прежде всего доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Рабочая группа
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Основные рекомендации
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций.
I. Определение, группы риска, классификация
Синдром диабетической стопы (СДС) объединяет патологические изменения периферической нервной системы, артериального и микроциркуляторного русла костно-суставного аппарата стопы, представляющие непосредственную угрозу развития язвенно-некротических поражений и гангрены стопы.
В группу риска развития СДС могут быть включены следующие группы лиц:
— Пациенты с нарушением периферической чувствительности любого генеза (уровень доказанности 2А).
— Лица с окклюзирующими заболеваниями периферических артерий (уровень доказанности 1В).
— Больные с деформациями стоп любого генеза (уровень доказанности 1А).
— Слепые и слабовидящие (уровень доказанности 2C).
— Одинокие пациенты и лица старческого возраста (уровень доказанности 2С).
— Злоупотребляющие алкоголем (уровень доказанности 2В).
Классификация синдрома диабетической стопы (Консенсус по диабетической стопе Diabetic Foot Study Group, 2011)
Выделяют следующие клинические формы синдрома диабетической стопы:
— Нейропатическая форма СДС:
— трофическая язва стопы;
— диабетическая остеоартропатия (ДОАП).
— Ишемическая форма СДС.
— Нейроишемическая форма СДС.
Классификация раневых дефектов у больных с синдромом диабетической стопы
Классификация PEDIS (Perfusion, Extent, Depth, Infection, Sensation), предложенная в 2003 г. и пересмотренная в 2011 г., учитывает не только глубину поражения мягких тканей (как было при использовании ранее разработанных классификаций), но и состояние периферического кровотока, иннервации, тяжесть инфекционного процесса. Ее использование предоставляет подробную информацию об имеющемся поражении врачам различных специальностей, занимающихся лечением пациента с синдромом диабетической стопы на различных этапах (хирургический и эндокринологический стационар, поликлиника).
II. Диагностика
Диагноз синдрома диабетической стопы основывается на результатах анализа анамнестических данных, осмотра нижних конечностей (состояние кожных покровов, наличие раневых дефектов и их характеристики, видимые деформации костных структур), данных оценки состояния периферической тактильной, вибрационной и температурной чувствительности, определении состояния периферического артериального кровотока.
Клиническая картина
Пациенты с СДС предъявляют жалобы на наличие длительно незаживающего раневого дефекта (иногда множественных дефектов) на стопе (возможно на обеих стопах). Длительность существования ран может колебаться от нескольких недель до 2–6 лет. Наличие и выраженность болевого синдрома зависят от состояния периферической чувствительности (возможно снижение вплоть до полной анестезии вследствие диабетической сенсорной нейропатии), уровня локальной ишемии и тяжести присоединившейся инфекции. При сборе анамнеза необходимо обратить внимание на длительность течения сахарного диабета (СД), наличие других поздних осложнений этого заболевания. Требуется помнить, что СД 2-го типа — скрытое, малосимптомное заболевание, которое часто диагностируется при обследовании пациента с уже развившимся тяжелым гнойно-некротическим поражением стопы. Также при сборе анамнеза необходимо обратить внимание на наличие сопутствующих, непосредственно не связанных с СД заболеваний, которые могут влиять на скорость заживления раневых дефектов (сердечная и дыхательная недостаточность, онкологические заболевания, алиментарная недостаточность, терапия глюкокортикоидами и иммуносупрессантами) (уровень доказанности 1А).
Осмотр и пальпация нижних конечностей. При осмотре стоп и голеней необходимо обратить внимание на состояние и цвет кожных покровов (сухие, влажные, бледные, розовые, гиперемированные), пальпаторно определить их температуру (холодные, теплые, горячие). Очень важно выявить асимметрию цвета и температуры кожи обеих стоп, что может служить первым признаком имеющегося нарушения. Необходимо оценить состояние ногтевых пластин, так как имеющийся онихомикоз может являться дополнительным источником инфекции. Результаты осмотра могут помочь составить первое мнение о возможной клинической форме синдрома диабетической стопы.
Оценка состояния периферического артериального кровотока. Клинически значимая артериальная недостаточность может быть исключена при наличии хорошо пальпируемого пульса на тыльной артерии стопы, передней и задней большеберцовых артериях или лодыжечно-плечевом индексе (ЛПИ) > 0,9. ЛПИ > 1,3 свидетельствует о ригидности артериальной стенки. У пожилых пациентов или у лиц с ЛПИ > 1,2 состояние артериального кровотока должно быть подтверждено уровнем артериального давления в пальцевой артерии (величиной пальце-плечевого индекса — ППИ) или данными транскутанной оксиметрии (ТсрО2 > 40 мм рт.ст.). Ультразвуковое дуплексное сканирование артерий подтверждает артериальную окклюзию, выявляет ее анатомическую локализацию и протяженность (уровень доказанности 1А).
Оценка состояния периферической иннервации. Наличие диабетической нейропатии устанавливается на основании определения тактильной чувствительности с помощью 10 г монофиламента (уровень доказанности 2А). Достоверность полученных результатов повышается при дополнительной оценке других видов чувствительности (вибрационной с помощью градуированного камертона 128 Гц или биотезиометра) и/или сухожильных рефлексов (уровень доказанности 2А).
Оценка состояния костных структур нижних конечностей. Золотым стандартом оценки состояния костей и суставов остается рентгенография, позволяющая с высокой достоверностью определять очаги остеолиза (остеомиелит) (уровень доказанности 1А). Мультиспиральная компьютерная томография позволяет уточнить локализацию и размеры остеомиелитического очага при планировании объема оперативного вмешательства (уровень доказанности 1А). Однако эти методы визуализации неинформативны в диагностике острой стадии диабетической остеоартропатии (ДОАП). В этом случае целесообразно использование магнитно-резонансной томографии; метод позволяет выявить отек костного мозга в зоне предполагаемого поражения (уровень доказанности 2А). Наиболее простым, доступным и достаточно информативным методом диагностики острой стадии ДОАП признается инфракрасная термометрия (уровень доказанности 2С). Разница температуры над пораженным и контралатеральным непораженным суставом в 2 и более градусов Цельсия позволяет с высокой долей вероятности диагностировать это осложнение и своевременно начать адекватное лечение.
Диагностика раневой инфекции. Основным методом диагностики инфекционного процесса в ране является бактериологическое исследование (уровень доказанности 1А). Для анализа необходимо брать образцы тканей из разных участков, так как микрофлора может различаться в разных областях дефекта. У пациентов с нейроишемической и ишемической формой СДС необходимо выявлять не только аэробные, но и анаэробные микроорганизмы и определять их чувствительность к современным антибактериальным препаратам. Клинически значимым считается содержание бактериальных тел выше 1 × 106 на 1 грамм ткани или обнаружение β-гемолитического стафилококка (уровень доказанности 1В).
Оценка состояния углеводного и липидного обмена является абсолютно необходимым компонентом обследования. Для этого необходимо исследование таких параметров, как уровень гликированного гемоглобина А1с (HbA1c), уровень пре- и постпрандиальной гликемии, общего холестерина, холестерина липопротеидов низкой плотности сыворотки крови. Коррекция нарушений углеводного обмена у больного с синдромом диабетической стопы должна проводиться параллельно с лечением раневого дефекта. Для пациентов с нейроишемической формой СДС обязательным является назначение гиполипидемической терапии статинами и нормализация артериального давления.
III. Лечение пациентов с синдромом диабетической стопы
Основным условием успешного лечения трофических язв у пациентов как с нейропатической, так и ишемической и нейроишемической формами синдрома диабетической стопы является обеспечение полной разгрузки пораженной области. Возможными методами разгрузки являются разгрузочный полубашмак, индивидуальная разгрузочная повязка и костыли (уровень доказанности 2В). Адекватное использование кресла-каталки не всегда возможно, особенно в амбулаторных условиях.
Индивидуальная разгрузочная повязка (Total Contact Cast) — наиболее эффективный метод разгрузки пораженной зоны стопы (уровень доказанности 1В).
Пациентам группы высокого риска развития трофических язв стоп (значимая артериальная недостаточность, тяжелая нейропатия, язвы стоп в анамнезе, грубый гиперкератоз) показано постоянное ношение профилактической обуви для больных диабетом (уровень доказанности 2С), а больным, перенесшим ампутацию в пределах стопы, — сложной ортопедической обуви (уровень доказанности 2А).
Параллельно с разгрузкой пораженной зоны должна проводиться первичная обработка раны (debridment), направленная на удаление всех некротизированных и нежизнеспособных тканей и подготовку раневого ложа к заживлению. Возможно использование хирургического, ферментного, механического, ультразвукового методов или их комбинации (уровень доказанности 1А). Метод обработки выбирается индивидуально, исходя из состояния раны, общего состояния больного, возможностей клиники. После проведения обработки рана должна быть закрыта стерильной атравматичной повязкой. В процессе лечения может возникнуть необходимость в повторном проведении обработки раневого дефекта.
Перед каждой сменой повязки рана должна быть промыта достаточным количеством (20–50 мл в зависимости от размера) стерильного физиологического раствора температурой 25–28 °С (уровень доказанности 2В).
Выбор повязки зависит от состояния локальной гемодинамики (наличия или отсутствия ишемии) и фазы раневого процесса. Выбранная повязка должна поддерживать влажную среду в ране (уровень доказанности 3А), контролировать уровень экссудата и препятствовать мацерации краев (уровень доказанности 1А). Она должна быть хорошо зафиксирована на ране, чтобы не травмировать ее за счет своей подвижности (уровень доказанности 2С).
Важнейшим аспектом лечения трофических язв у больных с синдромом диабетической стопы служит контроль раневой инфекции. Первым этапом является полное удаление некротизированных и нежизнеспособных тканей хирургическим методом (уровень доказанности 1В). Могут быть использованы как классический метод хирургической обработки, так и современные технологии (гидрохирургическое оборудование, ультразвуковая кавитация) (уровень доказанности 1В). При наличии критической ишемии конечности проведение хирургической обработки раны опасно, так как может привести к расширению зоны некроза. В случае проведения адекватной обработки раневого дефекта эпителизация должна начаться в течение 2 недель, при условии соблюдения оптимального режима разгрузки пораженной области. Если этого не произошло, показано проведение бактериологического исследования тканей раны (уровень доказанности 2С). Дальнейшие терапевтические мероприятия будут зависеть от результатов исследования. При выявлении β-гемолитического стафилококка и/или содержания микробных тел более 1 × 106 на 1 грамм ткани показаны повторная хирургическая обработка раневого дефекта и местное использование антисептика. При достижении бактериального баланса применение антисептика должно быть прекращено во избежание цитотоксического эффекта и бактериальной резистентности (уровень доказанности 1В). В качестве антисептика не должны использоваться спирт–содержащие жидкости, растворы кислот и щелочей, красящие вещества.
При активном инфекционном процессе (фебрильная лихорадка, лейкоцитоз, гнойный раневой экссудат, гиперемия и гипертермия мягких тканей пораженной области) показано проведение системной антибактериальной терапии с учетом характера и чувствительности микрофлоры (уровень доказанности 1А).
Важным условием при выборе антибактериального препарата является предварительная оценка азотовыделительной функции почек (по скорости клубочковой фильтрации — СКФ). При СКФ < 45 мл/мин/1,73 м2 доза антибактериального препарата должна быть редуцирована. Пациентам даже с начальными проявлениями диабетической нефропатии (на стадии микроальбуминурии) абсолютно противопоказаны препараты из группы аминогликозидов, амфотерицин В и некоторые цефалоспорины первого поколения (гентамицин, тобрамицин, амикацин, нетилмицин) (уровень доказанности 1В).
При подозрении на наличие остеомиелита должно быть выполнено дополнительное обследование (зондирование раны, рентгенография, МСКТ). При подтверждении диагноза показано хирургическое лечение — удаление пораженной кости с последующей антибактериальной терапией в течение 2–4 недель (уровень доказанности 2В).
После достижения бактериального баланса раны и заполнения ее объема здоровой грануляционной тканью на 75 % и более возможно выполнение пластического закрытия раны местными тканями или аутодермопластики (уровень доказанности 2С).
Необходимо регулярно последовательно документировать состояние раны (локализация, размеры, раневое дно, отделяемое, состояние окружающей кожи, выраженность болевого синдрома) и определение скорости заживления и оценки эффективности лечения. В том случае, если раневой дефект за 4 недели не сократился на 40 %, тактика лечения должна быть пересмотрена (уровень доказанности 2С).
Пациенты с ишемией конечности нуждаются в проведении реваскуляризирующих вмешательств (уровень доказанности 2А). Показаниями к ангиохирургическому вмешательству (баллонная ангиопластика, баллонная ангиопластика со стентированием, гибридные операции) являются гемодинамически значимые (> 85 %) стенозы и/или окклюзии артерий нижних конечностей, ведущие к ишемии мягких тканей стопы (ТсрО2 < 30 мм рт.ст.). В периоперационном периоде необходимо проводить профилактику контрастиндуцированной нефропатии. Для этого накануне вмешательства и после его проведения пациентам группы риска (хроническая болезнь почек 2-й ст. и выше) нужно отменить метформин, петлевые диуретики и ввести 1000 мл физиологического раствора внутривенно капельно (уровень доказанности 1В). При наличии гнойно-некротического очага его первичная санация должна быть выполнена до ангиохирургического вмешательства.
При невозможности выполнения реваскуляризирующего вмешательства показано назначение препаратов простагландинового ряда (уровень доказанности В).
Лечение диабетической остеоартропатии. В острой стадии ДОАП необходимо начать иммобилизацию пораженной конечности с помощью индивидуальной разгрузочной повязки (Total Contact Cast) в максимально ранние сроки (в день установления диагноза) (уровень доказанности 1А). Больным с хронической стадией ДОАП показано постоянное ношение сложной ортопедической обуви (уровень доказанности 3А).
Коррекция сахароснижающей терапии. При наличии показаний (превышение индивидуальных целевых показателей углеводного обмена) коррекция терапии должна проводиться параллельно с лечением трофической язвы стопы (уровень доказанности 3А).
При интенсификации лечения необходимо проводить профилактику тяжелых гипогликемических состояний (уровень доказанности 1В).
Пациенты с нейроишемической и ишемической формой СДС нуждаются в коррекции возможной дислипидемии, а больные после выполненной ангиопластики — в приеме антитромботиков в течение 6 мес.
При отсутствии заживления на фоне стандартной терапии можно использовать адъювантные методы (факторы роста, отрицательное давление, электростимуляция) (уровень доказанности 1В). В отечественной клинической практике доступными являются препараты на основе тромбоцитарного и эпидермального ростовых факторов. Они доказали свою эффективность в лечении трофических язв у больных с синдромом диабетической стопы (уровень доказанности 2А). Использование отрицательного давления (NPWT) возможно у пациентов с нейропатической и нейроишемической (после восстановления кровотока) формой синдрома. Абсолютно противопоказано использование NPWT у больных с выраженной ишемией конечности (TcpO2 < 30 мм рт.ст.), остеомиелитом, флегмоной и гангреной стопы (уровень доказанности 1В).
IV. Профилактика рецидивов трофических язв стоп у больных сахарным диабетом
Необходимым условием профилактики рецидивов трофических язв у больных с синдромом диабетической стопы является обеспечение преемственности и мультидисциплинарного подхода в организации длительного наблюдения за данной категорией пациентов.
Профилактическую роль играет индивидуальное обучение пациентов с уже имеющимися раневыми дефектами и/или высоким риском их развития, а также (при необходимости) их родных и близких, правилам ухода за ногами (уровень доказанности 2С).
Для предотвращения рецидивов трофических язв больные группы высокого риска трофических язв стоп должны постоянно (дома и на улице) пользоваться профилактической, а при необходимости — сложной ортопедической обувью (уровень доказанности 2С). Показанием для назначения сложной ортопедической обуви являются хроническая стадия диабетической остеоартропатии, ампутации достаточно большого объема (переднего отдела стопы, нескольких пальцев). Адекватность изготовленной ортопедической обуви должна регулярно оцениваться лечащим врачом (эндокринологом, хирургом, специалистом кабинета диабетической стопы) и меняться не реже 1 раза в год.
Частоту рецидивов уменьшает и ежедневный осмотр стоп пациентом (или его родственником), соблюдение правил ухода за ногами. Важную роль играют процедуры профессионального подиатрического ухода, которые должны осуществляться специально обученной медицинской сестрой в условиях кабинета диабетической стопы (уровень доказанности 2А).
Список литературы
1. Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под ред. И.И. Дедова, М.В. Шестаковой. — М., 2013. — 120 с.
2. Сахарный диабет. Острые и хронические осложнения / Под ред. И.И. Дедова, М.В. Шестаковой. — М., 2011. — 477 с.
3. Удовиченко О.В., Бублик Е.В., Максимова Н.В., Пряхина К.Ю., Ермолаева О.С., Спруит П., Галстян Г.Р. Эффективность иммобилизирующих разгрузочных повязок Total Contact Cast: обзор зарубежных рандомизированных клинических исследований и собственные данные // Сахарный диабет. — 2010. — № 2. — С. 50-55.
4. Abbott C.A., Malik R.A., van Ross E.R., Kulkarni J., Boulton A.J. Prevalence and characteristics of painful diabetic neuropathy in a large community-based diabetic population in the U.K. // Diabetes Care. — 2011 Oct. — № 34(10). — Р. 2220-4.
5. Alavi A., Sibbald R.G., Mayer D., Goodman L., Botros M., Armstrong D.G., Woo K., Boeni T., Ayello E.A., Kirsner R.S. Diabetic foot ulcers: Part I. Pathophysiology and prevention // J. Am. Acad. Dermatol. — 2014 Jan. — № 70(1). — 1.e1-18.
6. Alavi A., Sibbald R.G., Mayer D., Goodman L., Botros M., Armstrong D.G., Woo K., Boeni T., Ayello E.A., Kirsner R.S. Diabetic foot ulcers: Part II. Management // J. Am. Acad. Dermatol. — 2014 Jan. — № 70(1). — 21.e1-24.
7. Armstrong D.G., Mills J.L. Toward a change in syntax in diabetic foot care: prevention equals remission // J. Am. Pod. Med. Assoc. — 2013. — № 103. — Р. 161-2.
8. Armstrong D.G. An overview of foot infections in diabetes // Diabetes Technol. Ther. — 2011 Sep. — № 13(9). — Р. 951-7.
9. Bakker K., Apelqvist J., Schaper N.C. Practical guidelines on the management and prevention of the diabetic foot 2011 // Diab. Metab. Res. Rev. — 2012. — № 28(Suppl. 1). — Р. 225-231.
10. Barshes N.R., Sigireddi M., Wrobel J.S., Mahankali A., Robbins J.M., Kougias P., Armstrong D.G. The system of care for the diabetic foot: objectives, outcomes, and opportunities // Diabet Foot Ankle. — 2013 Oct 10. — № 4. Doi: 10.3402/dfa.v4i0.21847. еCollection 2013.
11. Bongaerts B.W., Rathmann W., Heier M., Kowall B., Herder C., Stöckl D. et al. Older subjects with diabetes and prediabetes are frequently unaware of having distal sensorimotor polyneuropathy: The KORA F4 study // Diabetes Care. — 2013. — № 36. — Р. 1141-6.
12. Bradbury A.W. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) trial in perspective // J. Vasc. Surg. — 2010. — № 51(5 Suppl.). — 1S-4S.
13. Cavanagh P.R., Bus S.A. Off-loading the diabetic foot for ulcer prevention and healing // Plast. Reconstr. Surg. — 2011 Jan. — № 127(Suppl. 1). — 248S-256S.
14. Clemens M.W., Attinger C.E. Angiosomes and wound care in the diabetic foot // Foot Ankle Clin. — 2010 Sep. — № 15(3). — Р. 439-64.
15. Dorresteijn J.A., Kriegsman D.M., Assendelft W.J., Valk G.D. Patient education for preventing diabetic foot ulceration // Cochrane Database Syst. Rev. — 2012. — № 10. — CD001488.
16. Edwards J., Stapley S. Debridement of diabetic foot ulcers // Cochrane Database Syst. Rev. — 2010. — CD003556.
17. Feinglass J., Shively V.P., Martin G.J., Huang M.E., Soriano R.H., Rodriguez H.E. et al. How «preventable» are lower extremity amputations? A qualitative study of patient perceptions of precipitating factors // Disabil. Rehabil. — 2012. — № 34. — Р. 2158-65.
18. Fincke B.G., Miller D.R., Christiansen C.L., Turpin R.S. Variation in antibiotic treatment for diabetic patients with serious foot infections: a retrospective observational study // BMC Health Serv. Res. — 2010. — № 10. — 193.
19. Frykberg R.G., Bevilacqua N.J., Habershaw G. Surgical off-loading of the diabetic foot // J. Vasc. Surg. — 2010. — № 52(3 Suppl.). — 44S-58.
20. Fusilli D., Alviggi L., Seghieri G., Bellis A. Improvement of diabetic foot care after the implementation of the International Consensus on the Diabetic Foot (ICDF): Results of a 5-year prospective study // Diabetes Res. Clin. Pract. — 2007. — № 75. — Р. 153-158.
21. Gordon K.A., Lebrun E.A., Tomic-Canic M., Kirsner R.S. The role of surgical debridement in healing of diabetic foot ulcers // Skinmed. — 2012 Jan-Feb. — № 10(1). — Р. 24-6.
22. Henry A.J., Hevelone N.D., Belkin M., Nguyen L.L. Socioeconomic and hospital-related predictors of amputation for critical limb ischemia // J. Vasc. Surg. — 2011. — № 53. — Р. 330-9.
23. Jones W.S., Patel M.R., Dai D., Subherwal S., Stafford J., Calhoun S. et al. Temporal trends and geographic variation of lower-extremity amputation in patients with peripheral artery disease: results from U.S. Medicare 2000–2008 // J. Am. Coll Cardiol. — 2012. — № 60. — Р. 2230-6.
24. Katon J.G., Reiber G.E., Nelson K.M. Peripheral neuropathy defined by monofilament insensitivity and diabetes status: NHANES 1999–2004 // Diabetes Care. — 2013 Jun. — № 36(6). — Р. 1604-6.
25. Landsman A., Agnew P., Parish L., Joseph R., Galiano R.D. Diabetic foot ulcers treated with becaplermin and TheraGauze, a moisture-controlling smart dressing: a randomized, multicenter, prospective analysis // J. Am. Podiatr. Med. Assoc. — 2010. — № 100. — Р. 155-60.
26. Lavery L.A., Higgins K.R., La Fontaine J., Zamorano R.G., Constantinides G.P., Kim P.J. Randomised clinical trial to compare total contact casts, healing sandals and a shear-reducing removable boot to heal diabetic foot ulcers // Int. Wound J. — 2014 Feb 21. Doi: 10.1111/iwj.12213. [Epub ahead of print]
27. Lewis J., Lipp A. Pressure-relieving interventions for treating diabetic foot ulcers // Cochrane Database Syst. Rev. — 2013 Jan 31. — № 1. — CD002302.
28. Lipsky B.A., Berendt A.R., Cornia P.B., Pile J.C., Peters E.J., Armstrong D.G., Deery H.G., Embil J.M., Joseph W.S., Karchmer A.W., Pinzur M.S., Senneville E. 2012 infectious diseases society of america clinical practice guideline for the diagnosis and treatment of diabetic foot infections // J. Am. Podiatr. Med. Assoc. — 2013 Jan-Feb. — № 103(1). — Р. 2-7.
29. López-de-Andrés A., Martínez-Huedo M.A., Carrasco-Garrido P., Hernández-Barrera V., Gilde-Miguel A., Jiménez-García R. Trends in lower-extremity amputations in people with and without diabetes in Spain, 2001–2008 // Diabetes Care. — 2011. — № 34. — Р. 1570-6.
30. Molines L., Darmon P., Raccah D. Charcot’s foot: newest findings on its pathophysiology, diagnosis and treatment // Diabetes Metab. — 2010 Sep. — № 36(4). — Р. 251-5.
31. Monteiro-Soares M., Martins-Mendes D., Vaz-Carneiro A., Sampaio S., Dinis-Ribeiro M. Classification systems for lower extremity amputation prediction in subjects with active diabetic foot ulcer: a systematic review and meta-analysis // Diabetes Metab. Res. Rev. — 2014 Feb 12. Doi: 10.1002/dmrr.2535. [Epub ahead of print]
32. Morbach S., Furchert H., Gröblinghoff U., Hoffmeier H., Kersten K., Klauke G.T., Klemp U., Roden T., Icks A., Haastert B., Rümenapf G., Abbas Z.G., Bharara M., Armstrong D.G. Long-term prognosis of diabetic foot patients and their limbs: amputation and death over the course of a decade // Diabetes Care. — 2012 Oct. — № 35(10). — Р. 2021-7. [Epub 2012 Jul 18]
33. Ndip A., Rutter M.K., Vileikyte L., Vardhan A., Asari A., Jameel M. et al. Dialysis treatment is an independent risk factor for foot ulceration in patients with diabetes and stage 4 or 5 chronic kidney disease // Diabetes Care. — 2010. — № 33. — Р. 1811-6.
34. Percival S.L., Hill K.E., Williams D.W., Hooper S.J., Thomas D.W., Costerton J.W. A review of the scientific evidence for biofilms in wounds // Wound Repair. Regen. — 2012 Sep-Oct. — № 20(5). — Р. 647-57.
35. Peters E.J., Lipsky B.A. Diagnosis and management of infection in the diabetic foot // Med. Clin. North Am. — 2013 Sep. — № 97(5). — Р. 911-46.
36. Pham H., Armstrong D.G., Harvey C., Harkless L.B., Giurini J.M., Veves A. Screening techniques to identify people at high risk for diabetic foot ulceration: a prospective multicenter trial // Diabetes Care. — 2000 May. — № 23(5). — Р. 606-11.
37. Potier L., Abi Khalil C., Mohammedi K., Roussel R. Use and utility of ankle brachial index in patients with diabetes // Eur. J. Vasc. Endovasc. Surg. — 2011. — № 41. — Р. 110-16.
38. Regenbogen S.E., Gawande A.A., Lipsitz S.R., Greenberg C.C., Jha A.K. Do differences in hospital and surgeon quality explain racial disparities in lower-extremity vascular amputations? // Ann Surg. — 2009. — № 250. — Р. 424-31.
39. Schaper N.C., Andros G., Apelqvist J., Bakker K., Lammer J., Lepantalo M. et al. Specific guidelines for the diagnosis and treatment of peripheral arterial disease in a patient with diabetes and ulceration of the foot 2011 // Diabetes Metab. Res. Rev. — 2012. — № 28(Suppl. 1). — Р. 236-7.
40. Schaper N.C., Apelqvist J., Bakker K. Reducing lower leg amputations in diabetes: a challenge for patients, healthcare providers and the healthcare system // Diabetologia. — 2012 Jul. — № 55(7). — Р. 1869-72.
41. Sibbald R.G., Ayello E.A., Alavi A., Ostrow B., Lowe J., Botros M., Goodman L., Woo K., Smart H. Screening for the high-risk diabetic foot: a 60-second tool (2012) // Adv. Skin Wound Care. — 2012 Oct. — № 25(10). — Р. 465-76; 477-8.
42. Snyder R.J., Cardinal M., Dauphinée D.M., Stavosky J. A post-hoc analysis of reduction in diabetic foot ulcer size at 4 weeks as a predictor of healing by 12 weeks // Ostomy Wound Manage. — 2010 Mar 1. — № 56(3). — Р. 44-50.
43. Snyder R.J., Kirsner R.S., Warriner R.A. 3rd, Lavery L.A., Hanft J.R., Sheehan P. Consensus recommendations on advancing the standard of care for treating neuropathic foot ulcers in patients with diabetes // Ostomy Wound Manage. — 2010 Apr. — № 56(4 Suppl.). — S1-24.
44. Sumpio B.E., Armstrong D.G., Lavery L.A., Andros G.; Society for Vascular Surgery; American Podiatric Medical Association. The role of interdisciplinary team approach in the management of the diabetic foot: a joint statement from the Society for Vascular Surgery and the American Podiatric Medical Association // J. Am. Podiatr. Med. Assoc. — 2010 Jul-Aug. — № 100(4). — Р. 309-11.
45. Taylor S.M., Johnson B.L., Samies N.L., Rawlinson R.D., Williamson L.E., Davis S.A., Kotrady J.A., York J.W., Langan E.M. 3rd, Cull D.L. Contemporary management of diabetic neuropathic foot ulceration: a study of 917 consecutively treated limbs // J. Am. Coll Surg. — 2011. — № 212(4). — Р. 532-548.
46. Wukich D.K., Armstrong D.G., Attinger C.E., Boulton A.J., Burns P.R., Frykberg R.G., Hellman R., Kim P.J., Lipsky B.A., Pile J.C., Pinzur M.S., Siminerio L. Inpatient management of diabetic foot disorders: a clinical guide // Diabetes Care. — 2013 Sep. — № 36(9). — Р. 2862-71.
47. Wukich D.K., Armstrong D.G., Attinger C.E., Boulton A.J., Burns P.R., Frykberg R.G., Hellman R., Kim P.J., Lipsky B.A., Pile J.C., Pinzur M.S., Siminerio L. Inpatient management of diabetic foot disorders: a clinical guide // Diabetes Care. — 2013 Sep. — № 36(9). — Р. 2862-71.
48. World Union of Wound Healing Societies (WUWHS) «Principles of best practice: Wound exudate and the role of dressings». A consensus document. — London: MEP Ltd., 2007.
49. World Union of Wound Healing Societies (WUWHS). Minimising pain at wound dressing-related procedures. A consensus document. — Toronto, Ontario, Canada: Wound Pedia Inc., 2007.

/105.jpg)
/106.jpg)