Журнал «Травма» Том 16, №3, 2015
Вернуться к номеру
Вертебральний больовий синдром: зв’язок із мінеральною щільністю та якістю кісткової тканини
Авторы: Поворознюк В.В., Орлик Т.В., Дзерович Н.І. - ДУ «Інститут геронтології ім. Д.Ф. Чеботарьова НАМН України», м. Київ
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
У статті наведені результати вивчення особливостей частоти та вираженості болю у грудному та поперековому відділах хребта в жінок у постменопаузальному періоді з різним станом мінеральної щільності кісткової тканини. Розраховано ризики розвитку болю в різних відділах хребта залежно від наявності вертебральних переломів і порушень структурно-функціонального стану кісткової тканини (остеопороз/остеопенія, зниження показника якості трабекулярної кісткової тканини). Висвітлено зв’язки між характеристиками вертебрального больового синдрому та показниками стану кісткової тканини.
В статье приведены результаты изучения особенностей частоты и выраженности боли в грудном и поясничном отделах позвоночника у женщин в постменопаузальном периоде с различным состоянием минеральной плотности костной ткани. Рассчитаны риски развития боли в разных отделах позвоночника в зависимости от наличия вертебральных переломов и нарушений структурно-функционального состояния костной ткани (остеопороз/остеопения, снижение показателя качества трабекулярной костной ткани). Освещены связи между характеристиками вертебрального болевого синдрома и показателями состояния костной ткани.
The article presents the results of studying the characteristics of the incidence and severity of thoracic and lumbar pain in postmenopausal women with a different state of bone mineral density. We have calculated the risks of pain in different parts of the spine, depending on the presence of vertebral fractures and disorders in the structural and functional state of the bone tissue (osteoporosis/osteopenia, decline in the trabecular bone score). The relationship between the characteristics of vertebral pain syndrome and indicators of bone health is considered.
біль у спині, мінеральна щільність кісткової тканини, якість трабекулярної кісткової тканини, вертебральні переломи, відносний ризик, жінки.
боль в спине, минеральная плотность костной ткани, качество трабекулярной костной ткани, вертебральные переломы, относительный риск, женщины.
back pain, bone mineral density, trabecular bone score, vertebral fractures, relative risk, women.
Статья опубликована на с. 56-61
Одним із найбільш поширених симптомів захворювань кістково–м’язової системи є біль, а серед больових синдромів — вертебральний больовий синдром. Поширеність болю у спині, за даними різних авторів, становить від 19 до 80 % усієї популяції [4, 7]. Найбільшу увагу у світовій літературі приділяють болю у нижній частині спини, який має серйозні медико–соціальні наслідки, оскільки розвивається переважно в осіб працездатного віку. За даними ряду досліджень, проведених у європейських країнах [7], найчастіше зустрічається біль у нижній частині спини та шийному відділі хребта, рідше — біль у грудному відділі. Хронічний персистуючий біль у нижній частині спини і шийному відділі спостерігається у 25–60 % пацієнтів протягом року після першого епізоду. Порівняльні дослідження [10] щодо поширеності болю у нижній частині спини показали, що 23 % пацієнтів із болем у попереку мають біль високої інтенсивності, що призводить до обмеження життєдіяльності та інвалідизації, порівняно з 15 % осіб із болем у грудному відділі [9]. Незалежно від причини та локалізації виникнення болю суттєво змінюються якість життя пацієнтів, рівень їх фізичної та життєвої активності.
Біль у спині може бути результатом численних захворювань кісток, м’яких тканин та інших органів і систем, часто він локалізований на відстані від дійсного вогнища патології. За даними ряду авторів, у жінок віком 45–60 років причинами больового синдрому в спині у 20 % випадків є дегенеративні процеси у міжхребетних дисках, у 19 % — спондилоартрити, у 15 % — сколіоз, спричинений різною довжиною кінцівок, у 14 % — ідіопатичний сколіоз, у 7 % — спондилолістез, у 6 % випадків — остеопороз і деформації тіл хребців [2, 8]. Незважаючи на доведеність і патогенетичну обґрунтованість багатьох захворювань і станів як причини болю у спині, на сьогодні залишається близько 15–20 % випадків болю у ділянці хребта, що не мають суттєвого підґрунтя для встановлення чіткого діагнозу.
Серед відомих факторів, що сприяють розвитку вертебрального больового синдрому, найбільшу роль відіграють вік, стать, фізичне навантаження, особливості професійної діяльності, надмірна маса тіла, менопауза [2]. Проте останнім часом у наукових дослідженнях особливу увагу приділяють менш вивченим предикторам, як–от: психологічний стан, рівень вітаміну D у сироватці крові, сімейний статус, стан кісткової та хрящової тканини.
Про роль стану кісткової тканини у розвитку болю в спині частіше за все говорять у випадках остеопорозу, ускладненого вертебральними переломами, наявність яких істотно впливає на захворюваність і летальність [1]. Найбільш складною є діагностика остеопорозу на перших стадіях захворювання, оскільки у більшості випадків першою клінічною ознакою захворювання є низькоенергетичний перелом. У зв’язку із цим останніми роками з’являється все більше нових діагностичних методів, що допомагають визначати групи ризику та ранню втрату кісткової тканини в різних груп населення.
Стан кісткової тканини залежить від багатьох факторів: мінеральної щільності кісткової тканини (МЩКТ), її метаболізму, мінералізації, макрогеометрії, мікроархітектури трабекулярної кісткової тканини, мікропереломів та ін. Однією з основних детермінант міцності кісткової тканини й ризику переломів є МЩКТ, за рахунок якої, за даними літератури, забезпечується 70–75 % міцності кістки [6]. Тим не менше використання даної методики у клінічній практиці має ряд обмежень. Одним з основних є значна зона перекриття в осіб, у яких розвиваються переломи та у яких не виникають. Наступним обмеженням використання МЩКТ є диспропорційна оцінка кортикального шару кістки залежно від обстежуваної ділянки за допомогою двофотонної рентгенівської абсорбціометрії і, відповідно, відмінність обміну кісткової тканини в досліджуваних зонах. Значимим обмеженням використання МЩКТ є також те, що вірогідні зміни показника на тлі лікування або віку можна оцінити після тривалого часу (зазвичай роки) [5]. Обмін у трабекулярній кістковій тканині відбувається значно швидше (у 8 разів вище порівняно з кортикальною). З огляду на це, оцінюючи мікроархітектуру трабекулярної кістки, збільшуємо точність і чутливість оцінки якості кісткової тканини й ризику переломів у клінічній практиці. Структуру трабекулярної кістки можна оцінити з використанням магнітно–резонансної томографії, комп’ютерної томографії, гістоморфометричного аналізу при біопсії кісткової тканини гребня здухвинної кістки, але ці методики є дорогими у використанні та не завжди доступні в клінічній практиці [13].
Метод оцінки якості трабекулярної кісткової тканини (trabecular bone score — TBS; TBS Insight, Med–Imaps) надає можливість аналізувати трабекулярну структуру відповідно до різних статистичних властивостей пікселів щодо щільності, внаслідок чого вираховується показник, який сильно корелює з 3D–параметрами проектованої трабекулярної кістки [5].
Показник TBS (L1–L4) з віком зменшується на 16 % у вікових групах від 45 до 90 років та негативно корелює з віком. Наявність остеоартриту хребта та його тяжкість незначно впливають на показник TBS та вірогідно — на МЩКТ на рівні поперекового відділу хребта. Вірогідні зміни якості трабекулярної кісткової тканини спостерігаються в жінок на більш ранньому терміні постменопаузального періоду — через 4 роки та більше, тоді як зміни МЩКТ визначаються при тривалості постменопаузального періоду 7 років і більше. Показник якості трабекулярної кісткової тканини є незалежним від МЩКТ та має важливу діагностичну цінність в оцінці структурно–функціонального стану кісткової тканини [11, 12].
У декількох перехресних дослідженнях встановлено, що TBS має зв’язок з остеопоротичними переломами тіл хребців, шийки стегнової кістки та переломів іншої локалізації у жінок у постменопаузальному періоді. Виявлено, що 73 % переломів спостерігались у жінок без остеопорозу, при цьому у 72 % жінок показник TBS був нижчим від середнього значення [13].
У попередніх дослідженнях в Україні встановлено, що показник TBS вірогідно негативно корелює з інтенсивністю болю у грудному та поперековому відділах хребта в жінок у постменопаузальному періоді; у розвитку вертебрального больового синдрому показник TBS відіграє суттєвішу роль, ніж показник МЩКТ. Також встановлено, що TBS корелює з наявністю переломів: на тлі найнижчих показників TBS розвивається 50,8 % вертебральних переломів, 43,7 % — периферичних і 32,8 % — комбінованої локалізації [3].
Враховуючи серйозне медико–соціальне значення остеопорозу та його ускладнень, апробація та впровадження нових методів оцінки структурно–функціонального стану кісткової тканини в осіб різного віку та статі у різних клінічних ситуаціях залишаються актуальними. Крім того, на сьогодні у світовій літературі немає даних щодо зв’язків показника TBS із вертебральним больовим синдромом, який у багатьох випадках супроводжує зниження показників структурно–функціонального стану кісткової тканини.
Мета: вивчити особливості вертебрального больового синдрому в жінок у постменопаузальному періоді залежно від характеристик структурно–функціонального стану кісткової тканини.
Об’єкт дослідження
На базі Українського науково–медичного центру проблем остеопорозу обстежено 589 жінок віком 45–89 років у постменопаузальному періоді. Залежно від показників мінеральної щільності кісткової тканини обстежені були розподілені на групи: остеопороз (ОП, n = 136), остеопенія (ОПн, n = 227) та норма за МЩКТ (норма, n = 226). Серед залучених у дослідження осіб 389 не мали низькоенергетичних переломів, 130 осіб мали вертебральні та 70 — невертебральні переломи, у зв’язку із чим аналіз проводили у групах у цілому та окремо у підгрупах з переломами та без них.
Методи дослідження
Наявність і вираженість болю у грудному та поперековому відділах хребта оцінювали за допомогою 4–компонентної 10–бальної візуально–аналогової шкали у балах від 0 до 10.
МЩКТ оцінювали на рівні поперекового відділу хребта (МЩКТ L1–L4) з використанням двохенергетичного рентгенівського денситометра Prodigy (GE Medical systems, Lunar, model 8743, 2005). Розподіл на групи залежно від показників МЩКТ проводили відповідно до критеріїв Всесвітньої організації охорони здоров’я: норма (Т–критерій > –1,0 SD), ОПн (–1,0 ≤ Т–критерій > –2,5 SD), ОП (Т–критерій ≤ –2,5 SD). Показник якості трабекулярної кісткової тканини визначали на рівні поперекового відділу хребта (TBS L1–L4) з використанням програмного забезпечення TBS Insight (Med–Imaps, Бордо, Франція; 2006) на тому ж двофотонному рентгенівському денситометрі. Залежно від показника якості трабекулярної кісткової тканини обстежених жінок було розподілено на групи (квартилі) (Q TBS L1–L4):
— Q–І — найнижчий квартиль (TBS = 0,362–1,077);
— Q–ІІ — нижній квартиль (TBS = 1,078–1,203);
— Q–ІІІ — верхній квартиль (TBS = 1,204–1,321);
— Q–ІV — найвищий квартиль (TBS = 1,322– 1,793).
Статистичний аналіз проводили з використанням пакетів програм Statistiсa 6.0 Copyright© StatSoft, Inc. 1984–2001, Serial number 31415926535897. Порівняння досліджуваних змінних у двох незалежних групах проводили за допомогою тесту Манна — Уїтні. Результати наведені у вигляді Me [LQ; UQ]. Кореляційні зв’язки визначали за допомогою непараметричного рангового коефіцієнта Спірмена (R). Відносний ризик (ВР) та відношення шансів (ВШ) обчислювали на основі таблиць кростабуляції за формулами: ВР = (а/А)/(с/В) і ВШ = (a•d)/(b•с). Для кожного з цих показників окремо визначався 95% довірчий інтервал (ДІ). Критичним рівнем значущості при перевірці статистичних гіпотез вважали р < 0,05.
Результати дослідження
Встановлено, що у пацієнток з ОП та нормою за МЩКТ частота болю у грудному відділі вірогідно не відрізняється між квартилями за TBS (x2 = 1,6; р = 0,65 та x2 = 2,9; р = 0,40 відповідно). У пацієнток з ОПн показник частоти болю у грудному відділі був вірогідно вищий у групах з низьким показником TBS (Q–І та Q–ІІ) порівняно з групою Q–ІІІ (відповідно x2 = 9,9; р = 0,05 та р = 0,02). Слід відзначити, що у пацієнток з ОП у групі Q–ІІІ показник частоти болю у грудному відділі був вірогідно вищим порівняно з ОПн (р = 0,04) та нормальною МЩКТ (р = 0,05) (рис. 1А).
Частота болю у поперековому відділі хребта в жінок у постменопаузальному періоді була вірогідно вищою у групах Q–І та Q–ІІ порівняно з групами Q–ІІІ та Q–ІV та не відрізнялась залежно від стану МЩКТ (рис. 1Б).
На основі отриманих результатів можна припустити, що частота болю у грудному відділі у хворих на ОП не залежить від показника TBS, у той час як у поперековому — є вищою на тлі низьких показників TBS незалежно від МЩКТ.
На наступному етапі було відокремлено пацієнтів, які мали переломи будь–якої локалізації. За результатами проведеного аналізу частоти болю у грудному та поперековому відділах хребта у жінок із різним станом TBS та МЩКТ встановлено суттєві відмінності від отриманих раніше результатів за показником частоти болю у грудному відділі у хворих на ОП. Так, у групі Q–І з ОП при відсутності переломів ризик розвитку болю у грудному відділі був вірогідно меншим (ВР = 1,9; 95% ДІ 1,05–4,39; р = 0,02). У групі Q–ІІ з ОП частота болю мала тенденцію до зменшення (ВР = 1,4; 95% ДІ 0,78–3,18; р = 0,07). У групах Q–ІІІ та Q–ІV частота болю у грудному відділі суттєво не змінювалась, але у групі Q–ІІІ була вірогідно вищою порівняно з Q–І (р = 0,03). А у жінок з ОПн та нормальною МЩКТ вірогідних відмінностей показників частоти болю у грудному відділі залежно від наявності переломів не виявлено. За розрахунком величини апроксимації (предиктора, R2) встановлено, що комбінація низьких показників TBS (Q–І, Q–ІІ) та високих МЩКТ (норма) або високих показників TBS (Q–ІV) та низьких МЩКТ (остеопороз) може пояснювати наявність болю у грудному відділі у близько 70 % випадків (рис. 2А).
Ризик розвитку болю у поперековому відділі у жінок без переломів вірогідно не змінювався в усіх групах за МЩКТ та TBS. Проте частота болю у даному відділі хребта залишалась вірогідно більшою у жінок з ОП у підгрупах Q–І, Q–ІІ та нормою у групі Q–І порівняно з відповідними підгрупами Q–ІV (р = 0,03 та р = 0,05 відповідно) (рис. 2Б).
На наступному етапі дослідження вивчали особливості інтенсивності болю у грудному та поперековому відділах хребта в жінок у постменопаузальному періоді залежно від показника TBS у квартильних підгрупах з переломами та без них.
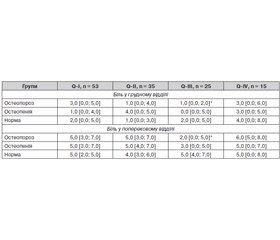
У пацієнток з ОП вираженість болю у грудному відділі була вірогідно більша на тлі високих показників TBS порівняно із хворими з ОП та низькими показниками TBS (Q–І, р < 0,05) і пацієнтами з ОПн та нормою з високими TBS (Q–ІІІ та Q–ІV, р < 0,05). Вираженість болю у поперековому відділі у жінок з ОП також була вірогідно більшою у групі Q–ІV порівняно з відповідною групою Q–І (р = 0,02). У пацієнток з ОПн вираженість болю у попереку була вірогідно більшою у групі Q–ІІ порівняно з відповідною групою Q–ІV (р = 0,04). А у жінок з нормою за МЩКТ — вірогідно більший рівень болю у поперековому відділі у групі Q–І порівняно з групами Q–ІІ, Q–ІІІ, Q–ІV (р < 0,05) (табл. 1).
Серед жінок із вертебральними переломами рівень болю у грудному та поперековому відділах вірогідно не відрізнявся залежно від стану МЩКТ та TBS, окрім хворих на ОП групи Q–ІІІ, у яких вираженість болю у грудному та поперековому відділах була вірогідно меншою порівняно з пацієнтками з ОП Q–ІV (табл. 2).
За результатами кореляційного аналізу зв’язків показника TBS у групах жінок у постменопаузальному періоді залежно від стану МЩКТ встановлено, що показник якості трабекулярної кісткової тканини в усіх досліджуваних групах за МЩКТ (остеопороз, остеопенія, норма) вірогідно негативно корелює з віком, масою тіла та індексом маси тіла, наявністю та вираженістю болю у поперековому відділі хребта, наявністю переломів та позитивно — з МЩКТ шийки стегнової кістки. Крім того, у пацієнток з остеопенією та нормою за МЩКТ встановлено вірогідний негативний зв’язок між TBS і тривалістю постменопаузального періоду та позитивний зв’язок з МЩКТ L1–L4 у хворих на остеопенію і рівнем 25(ОН)D у сироватці крові у хворих з нормальною МЩКТ (табл. 3).
Таким чином, у жінок у постменопаузальному періоді на тлі низьких показників якості трабекулярної кісткової тканини вірогідно більша частота болю у поперековому відділі незалежно від стану МЩКТ, що, на нашу думку, може бути пов’язано зі статико–динамічним навантаженням (яке у поперековому відділі більше, ніж у грудному) на тлі слабкої трабекулярної структури (найнижчі показники TBS), що сприяє розвитку больового синдрому за рахунок перенапруження трабекул і, як наслідок, мікротріщин у кісткових балках.
Дисбаланс мінеральної щільності та якості кісткової тканини (низькі показники TBS на тлі високих МЩКТ, або навпаки) можуть пояснювати близько 70 % випадків наявності болю у грудному відділі у жінок у постменопаузальному періоді без низькоенергетичних переломів.
У хворих на остеопороз та остеопенію на тлі низьких показників TBS вірогідно збільшується ризик розвитку болю у грудному відділі (у 1,4–1,9 раза) за наявності низькоенергетичних переломів будь–якої локалізації.
Наявність болю у грудному та/чи поперековому відділах хребта на тлі зниження показника якості трабекулярної кісткової тканини може слугувати раннім маркером втрати кісткової маси та спонукати до додаткового обстеження жінок і застосування профілактичних заходів щодо розвитку остеопенії/остеопорозу.
1. Корж Н.А., Поворознюк В.В., Дедух Н.В., Зупанец И.А. Остеопороз: клиника, диагностика, профилактика и лечение. — Х.: Золотые страницы, 2002. — 468 с.
2. Поворознюк В.В. Захворювання кістково–м’язової системи в людей різного віку (вибрані лекції, огляди, статті): У 4 т. — К., 2015.
3. Поворознюк В.В., Дзерович Н.І., Орлик Т.В. Показник якості трабекулярної кісткової тканини в клінічній практиці: огляд літератури та результати власних досліджень // Проблеми остеології. — 2014. — 17, № 2. — С. 3–14.
4. Andersson H.I. The epidemiology of chronic pain in a Swedish rural area // Qual Life Res. — 1994. — Suppl. 1. — S. 19–26.
5. Cormier C., Lamy O., Poriau S. TBS in routine clinical practice: proposals of use // Atlas of TBS use. Edition 2012. — 2012. — 16 p.
6. Hans D., Winzenrieth R. Estimation of bone microarchitecture pattern from AP spine DXA scans using the trabecular bone score (TBS): аn added value in clinical routine for the patient. A short review // Osteologický bulletin. — 2011. — 16(3). — P. 70–78.
7. Juniper M., Le T.K., Mladsi D. The epidemiology, economic burden, and pharmacological treatment of chronic low back pain in France, Germany, Italy, Spain and the UK: a literature–based review // Expert. Opin. Pharmacother. — 2009. — 12. — Р. 2581–2592.
8. Kann P., Schulz G., Schehler B., Beyer J. Backache and osteoporosis in perimenopausal women // Med. Klin. — 1993. — 88(1). — P. 9–15.
9. Manchikanti L., Singh V., Datta S. et al. American Society of Interventional Pain Physicians. Comprehensive review of epidemiology, scope, and impact of spinal pain // Pain Physician. — 2009. — 12(4). — Р. 35–70.
10. Niemelainen R., Videman T., Battie M.C. Prevalence and characteristics of upper or mid–back pain in Finnish men // Spine. — 2006. — 12. — Р. 1846–1849.
11. Pothuaud L., Barthe N., Krieg M.–A. Evaluation of the potential use of trabecular bone score to complement bone mineral density in the diagnosis of osteoporosis: a preliminary spine BMD e matched, Case–control study // Journal of Clinical Densitometry: Assessment of Skeletal Health. — 2009. — 12(2). — P. 170–176.
12. Silva B.C., Leslie W.D., Resch H. et al. Trabecular bone score: a noninvasive analytical method based upon the DXA image // Journal of Bone and Mineral Research. — 2014. — 29(3). — P. 518–530.
13. Winzenrieth R., Dufour R., Pothuaud L. et al. A retrospective case–control study assessing the role of trabecular bone score in postmenopausal caucasian women with osteopenia: analyzing the odds of vertebral fracture // Calcif. Tissue Int. — 2010. — 86. — P. 104–109.

/58/58.jpg)
/59/59.jpg)
/59/59_2.jpg)
/60/60.jpg)