Журнал «Травма» Том 16, №3, 2015
Вернуться к номеру
Результати ендопротезування великих суглобів у хворих з пухлинами кісток та причини ускладнень
Авторы: Проценко В.В., Дуда Б.С., Салманова К.М. - ДУ «Інститут травматології та ортопедії НАМН України», м. Київ
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Вивчені результати ендопротезування великих суглобів при пухлинах кісток у 117 пацієнтів. Хворим були імплантовані вітчизняні індивідуальні онкологічні ендопротези та закордонні моделі модульних ендопротезів. У 42 (35,9 %) пацієнтів у різні строки після первинного онкологічного ендопротезування виникли ускладнення, у 28 з них було виконано реендопротезування. Найбільш частими ускладненнями після ендопротезування були: інфекційні — 18 (15,4 %) випадків, асептичне розхитування ніжки ендопротеза — 18 (15,4 %). Рецидиви пухлини виявлено у 10 (8,5 %) хворих. Причинами ускладнень після операцій ендопротезування були: попередньо виконане хірургічне втручання, попередньо проведена променева терапія, локалізація пухлини, об’єм видаленої пухлини, довжина резеційованого фрагмента кістки по відношенню до довжини кістки в цілому, тривалість операції, об’єм крововтрати під час операції, конструкція ендопротеза та техніка його встановлення.
Изучены результаты эндопротезирования крупных суставов при опухолях костей у 117 пациентов. Больным были имплантированы отечественные индивидуальные онкологические эндопротезы и зарубежные модели модульных эндопротезов. У 42 (35,9 %) пациентов в различные сроки после первичного онкологического эндопротезирования возникли осложнения, у 28 из них было выполнено реэндопротезирование. Наиболее частыми осложнениями после эндопротезирования были: инфекционные — 18 (15,4 %) случаев, асептическое расшатывание ножки эндопротеза — 18 (15,4 %). Рецидивы опухоли выявлены у 10 (8,5 %) больных. Причинами осложнений после операций эндопротезирования являлись: предварительно выполненное хирургическое вмешательство, предшествующая лучевая терапия, локализация опухоли, объем удаленной опухоли, длина резецированного фрагмента кости по отношению к длине кости в целом, продолжительность операции, объем кровопотери во время операции, конструкция эндопротеза и техника его установки.
The results of large joint replacement in bone tumors were studied in 117 patients. Patients underwent implantation with the use of domestic individual oncological implants and foreign models of modular prostheses. In 42 (35.9 %) patients at different periods after the primary cancer arthroplasty, there were observed complications, 28 of them underwent re-replacement. The most common complications after replacement were: infectious — 18 (15.4 %) cases, aseptic loosening of the prosthesis stem — 18 (15.4 %). Tumor recurrences were detected in 10 (8.5 %) patients. Causes of complications after replacement were: previous surgery, previous radiotherapy, tumor localization, size of the removed tumor, the length of the resected bone fragments relative to the whole length of the bone, the duration of surgery, blood loss during surgery, construction of endoprosthesis and technique of its installation.
пухлини кісток, онкологічні ендопротези, ендопротезування суглобів, причини ускладнень ендопротезування, ревізійне ендопротезування.
опухоли костей, онкологические эндопротезы, эндопротезирование суставов, причины осложнений эндопротезирования, ревизионное эндопротезирование.
bone tumors, oncological implants, joint replacement, causes of arthroplasty complications, revision arthroplasty.
Статья опубликована на с. 39-44
Вступ
До 70–х років минулого сторіччя при пухлинному ураженні кісток кінцівки операцією вибору була ампутація або екзартикуляція кінцівки [21]. На даний час світовий стандарт лікування хворих із злоякісними пухлинами кісток — комбінований або комплексний підхід, одним з етапів якого є хірургічне лікування. Завдання ортопеда при виконанні операції полягає в радикальності оперативного втручання з подальшим забезпеченням адекватної якості життя пацієнта. Існує декілька основних методик реконструкцій після проведення сегментарної резекції кістки: алотрансплантація, автотрансплантація та ендопротезування. Аналіз вітчизняної та зарубіжної літератури показав, що авто– й алотрансплантація мають право на існування й застосовуються рядом клінік [5, 14, 19, 20], але на даний час 90 % пацієнтів зі злоякісними ураженнями довгих кісток виконується органозберігаюче хірургічне лікування в обсязі сегментарної резекції з ендопротезуванням [1, 2]. Заміщення дефектів кісток онкологічними ендопротезами стало можливим у другій половині ХХ сторіччя. Це стало можливим завдяки використанню нових технологій лікування й застосуванню нових конструкцій ендопротезів [9, 17].
В онкоортопедії при ендопротезуванні використовуються різні моделі й конструкції ендопротезів, у тому числі як цементні, так і безцементні системи, і в більшості випадків застосовуються нестандартні ендопротези [5, 13, 15, 18].
Перевагою ендопротезування, на відміну від інших методів реконструкції, є одномоментна компенсація імплантатом масивних кісткових дефектів при збереженні опороздатності та рухів у суглобі, що забезпечує відновлення функції кінцівки, покращує результати органозберігаючих операцій та поліпшує якість життя пацієнта [9, 11]. За даними ряду авторів, ендопротезування хоча й покращує функціональні, онкологічні та психологічні результати протипухлинного лікування, але не впливає на прогноз захворювання [2, 12].
Зі зростанням хірургічної активності на користь органозберігаючих операцій у вигляді ендопротезування суглобів зростає й кількість ускладнень, характерних для ендопротезування. Серед них переважають інфекційні ускладнення (3–13 %) і різні види нестабільності ендопротеза та його вузлів, що становлять від 2 до 10 % [11, 18].
Загальна частота інфекційних ускладнень ендопротезування великих суглобів у онкологічних хворих становить 10 %, ранніх — 57,6 % та пізніх — 13,6 % [7, 8]. Ліквідувати ці ускладнення консервативними заходами, що включають системне та місцеве введення антибіотиків, активне дренування рани, видалення імплантатів та кісткового цементу, застосування одноетапного реендопротезування, вдається лише в 27–30 % хворих [3]. Одним із протипоказань при ендопротезуванні є неможливість адекватного формування м’язового футляра імплантата, тому що це збільшує ризик інфекційних ускладнень і тим самим погіршує функціональні результати [10].
Механічні ускладнення, що виникають після ендопротезування суглобів, також мають велике значення: значна травматизація м’яких тканин, нерівномірність розподілу навантаження на кістку, некроз кістки внаслідок механічної обробки, висока температура полімеризації цементу, реакція організму на сторонній предмет, вузол тертя в штучному суглобі, мікрорухомість ендопротеза та його компонентів унаслідок неадекватної фіксації призводять до асептичної нестабільності ендопротезу [4, 6, 16].
Отже, ускладнення після ендопротезування суглобів є значною проблемою, що веде до порушення функції, а іноді й до втрати кінцівки, значно погіршує якість життя хворих, яким виконано ендопротезування суглоба з приводу пухлин довгих трубчастих кісток. Дотепер недостатньо визначені основні фактори, що впливають на виникнення ускладнень. У даній статті ми наводимо результати ендопротезування великих суглобів у хворих з пухлинами кісток та аналізуємо причини ускладнень.
Матеріали та методи
За період з 2009 по 2015 рік у клінічному відділі ДУ «Інститут травматології та ортопедії НАМНУ» виконано 117 органозберігаючих операцій при пухлинах кісток в об’ємі сегментарної резекції з наступним ендо– або реендопротезуванням великих суглобів та діафізів кісток. Середній вік хворих становив 40,4 ± 1,5 року (від 10 до 79 років), жінок було 60 (51,3 %), чоловіків — 57 (48,7 %).
Хворим були імплантовані різні види ендопротезів. 90 хворим імплантовані вітчизняні індивідуально виготовлені онкологічні ендопротези НВО «Інмед», 27 хворим імплантовані закордонні модульні ендопротези (16 — фірми Stryker (CША), 9 — фірми Valdemar Link (Німеччина), 1 — «Безноска» (Чехія), 1 — «Імпланкаст» (Німеччина)). У табл. 1 подані морфологічні форми пухлин, що зустрічалися.
Об’єм хірургічного втручання залежав від локалізації пухлини: хворим виконувалася резекція суглобового сегмента або діафіза кістки з пухлиною та заміщення дефекту ендопротезом або металевим імплантом. У табл. 2 подана кількість випадків ендопротезування суглобів та діафізів кісток.
Абластичне видалення пухлини суглобового або діафізарного сегмента спонукало виконувати широку резекцію новоутворення. При ендопротезуванні кісток та суглобів дотримувалися основних принципів онкохірургії — футлярності та абластичності, видалення одним блоком зони біопсії, виконували адекватну м’язову пластику, закриваючи ендопротез м’якими тканинами для зниження ризику ускладнень. З метою профілактики металозу та для фіксації м’язів ми використовували полімерні туби фірми Mutars (Німеччина), які мають підвищену тропність до м’яких тканин, що сприяє швидкому рубцюванню й відновленню природної точки прикріплення м’язів. Залежно від конкретних анатомо–функціональних змін застосовувалися спеціальні конструкції імплантів, інструментарій та методичні прийоми, що доповнювали стандартну техніку операцій. При ендопротезуванні використовували цементний тип фіксації ендопротеза.
У всіх випадках під час операції ендопротезування проводився замір об’єму видаленого препарату та довжини резеційованого кісткового фрагмента, враховувалися тривалість наркозу та об’єм крововтрати під час операції, що також впливало на розвиток післяопераційних ускладнень.
Об’єм видаленого препарату у хворих становив: від 72 до 150 см3 — 46 випадків, від 150 до 320 см3 — 70, від 320 до 480 см3 — 1. Довжина резеційованого кісткового фрагмента з пухлиною була: від 90 до 150 мм — 68 випадків, від 150 до 250 мм — 48, від 250 до 340 мм — 1. Тривалість наркозу: до 2,5 години — 18 випадків, 2,5–3,5 години — 38, понад 3,5 години — 61. Об’єм крововтрати під час операції: 300–500 мл — 39 випадків, 500–1000 мл — 73, понад 1000 мл — 5.
У 23 (19,66 %) хворих до операції відзначався патологічний перелом, що істотно ускладнювало передопераційне обстеження та створювало додаткові технічні складності під час операції та при подальшій реабілітації.
У 15 (12,82 %) хворих до операції ендопротезування за місцем проживання були виконані різні хірургічні втручання, що теж відігравало роль у виникненні післяопераційних ускладнень, 54 (46,15 %) пацієнтам у передопераційному періоді проведені курси внутрішньовенної та внутрішньоартеріальної поліхіміотерапії, 21 (17,95 %) хворому в передопераційному періоді проведені курси променевої терапії від 30 до 40 Грей на пухлину кістки.
Функціональний результат прооперованої кінцівки визначався за шкалою MSTS (Musculosceletal Tumor Society Staging System). Якість життя хворих визначалась у балах згідно з питальником EORTC QLQ–30. Виживаність хворих визначалась за методом Kaplan — Meier.
Отримані результати лікування
У результаті ендопротезування великих суглобів 117 хворим ортопедичні ускладнення спостерігалися у 42 (35,9 ± 0,26 %) пацієнтів (р > 0,05), рецидиви пухлини — у 10 (8,5 ± 0,1 %) пацієнтів (р > 0,05). Ортопедичні ускладнення були розділені нами на 2 групи: 1–ша група (інфекційні) — інфекційні ускладнення післяопераційної рани, 2–га група (механічні) — асептична нестабільність ендопротеза, руйнування конструкції ендопротеза, а також переломи кісток у місці імплантації ніжок ендопротеза. Окрему групу становили онкологічні ускладнення — рецидиви пухлини.
Інфекційні ускладнення спостерігались у 18 (15,40 ± 0,14 %) пацієнтів (р > 0,05) у строки від 28 діб до 5,6 року. Інфекційні ускладнення відзначались після ендопротезування колінного суглоба у 14 випадках, кульшового — у 3, ліктьового — в 1. У 8 випадках вдалося ліквідувати запальний процес та зберегти первинно встановлений ендопротез шляхом діалізу та проведення антибіотикотерапії. У 7 пацієнтів після видалення компонентів ендопротеза та кісткового цементу виконували радикальну хірургічну обробку рани з видаленням усіх патологічно змінених тканин, промиванням рани розчинами антисептиків та встановленням металоцементного спейсера з наступним реендопротезуванням суглоба через 6–9 місяців (при позитивних контрольних посівах рідини на мікрофлору з місця встановлення спейсера), у 3 пацієнтів, у яких запальний процес не вдалося ліквідувати, виконано ампутацію кінцівки.
Механічні ускладнення: асептична нестабільність компонентів ендопротеза зареєстрована у 18 (15,40 ± 0,14 %) пацієнтів (р > 0,05) у строки від 8 місяців до 5 років. Асептична нестабільність розвинулась після резекції дистального відділу стегнової кістки у 8 пацієнтів, проксимального відділу великогомілкової — у 6, проксимального відділу стегнової кістки — у 2, проксимального відділу плечової кістки — в 1, дистального відділу плечової кістки — в 1. Кількість ревізій при даному типу ускладнень: після встановлення індивідуально виготовлених імплантатів фірми «Інмед» — 16 (13,7 %), при використанні модульних ендопротезів — 2 (1,7 %). У 16 випадках пацієнтам виконано реендопротезування із заміною тільки одного компонента ендопротеза та у 2 (1,7 %) пацієнтів — із заміною обох компонентів ендопротеза. Руйнування конструкції ендопротеза спостерігалось у 3 (2,60 ± 0,06 %) пацієнтів (р > 0,05) у строки від 3 до 5,4 року через проблеми, пов’язані із самою конструкцією ендопротеза. Руйнування ендопротеза фірми «Інмед» сталося у 2 (1,7 %) випадках, ендопротеза «Безноска» — в одному (0,9 %). Перелом кістки в місці імплантації ніжки ендопротеза спостерігався у 3 (2,60 ± 0,06 %) пацієнтів (р > 0,05). Цим хворим виконано металоостеосинтез місця перелому за допомогою металевих пластин та дротяних серкляжів.
Онкологічні результати: рецидиви пухлини виявлені в 10 (8,50 ± 0,06 %) хворих (р > 0,05) у строки від 19 до 56 місяців, в 1 хворого виконано видалення рецидиву пухлини, 3 пацієнтам виконано ампутацію нижньої кінцівки на рівні середньої третини стегна, 3 хворим виконано екзартикуляцію нижньої кінцівки в кульшовому суглобі, у 3 хворих на тлі рецидиву пухлини з множинними метастазами в легені проводились курси поліхіміотерапії та променевої терапії.
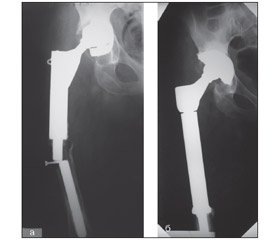
Наводимо приклади рентгенограм хворих (рис. 1–3), яким виконано ендопротезування та реендопротезування з приводу різних ускладнень.
/41/41.jpg)
Функціональний результат кінцівки (за шкалою MSTS) після ендопротезування кульшового суглоба становив 80,00 ± 0,07 % (p > 0,05), після ендопротезування діафіза стегнової кістки — 94,00 ± 0,05 % (p > 0,05), після резекції дистального відділу стегнової кістки та ендопротезування колінного суглоба — 90,00 ± 0,05 % (p > 0,05), після резекції проксимального відділу великогомілкової кістки та ендопротезування колінного суглоба — 75,00 ± 0,08 % (p > 0,05), після ендопротезування діафіза великогомілкової кістки — 92,00 ± 0,05 % (p > 0,05), після ендопротезування надступаково–гомілкового суглоба — 70,00 ± 0,09 % (p > 0,05), після ендопротезування плечового суглоба — 70,00 ± 0,09 % (p > 0,05), після ендопротезування діафіза плечової кістки — 96,00 ± 0,05 % (p > 0,05), після ендопротезування ліктьового суглоба — 75,00 ± 0,08 % (p > 0,05).
Якість життя хворих за опитувальником EORTC QLQ–30 підвищилась з 40–50 балів до ендопротезування і становила в середньому 75–80 балів після ендопротезування.
Загальна трирічна виживаність пацієнтів становила 82,20 ± 0,14 % (p > 0,05), п’ятирічна — 65,80 ± 0,26 % (p > 0,05).
Обговорення результатів
Аналіз даних переконливо показує, що якщо до операції ендопротезування хворим вже було виконано хірургічне втручання або проводилась променева терапія, то це підвищує ризик виникнення післяопераційних ускладнень.
При цьому найвищі показники гнійно–запальних ускладнень були в групі хворих, у яких проводилася передопераційна променева терапія, — 33,3 %.
Локалізація пухлини, з приводу якої виконувалося ендопротезування, також відігравала важливу роль у виникненні ускладнень. Найнебезпечнішою локалізацією була проксимальна частина великогомілкової кістки — 24 % ускладнень, при ендопротезуванні цієї зони завжди відзначався дефіцит м’яких тканин, що потребувало м’язової пластики.
Асептичне розхитування, як правило, обумовлене реактивною перебудовою та резорбцією кістки у відповідь на змінне навантаження, що врешті–решт призводить до асептичної нестабільності ендопротеза. У нашому дослідженні дане ускладнення розвинулось у 18 (15,4 %) пацієнтів. Цей показник дещо нижче за показники, подані в літературі: А.Л. Баранецький — 27,3–31 % [6]; А.А. Бабалаев зі співавторами — 25 % [4]; E.R. Henderson зі співавторами — 19 % [16], але строки спостережень в нашому дослідженні коротші.
Об’єм видаленої пухлини варіював від 72 до 480 см3. Найбільше випадків ускладнень було в групі хворих з об’ємом видаленої пухлини від 150 до 250 см3 — 17 (24,3 %), причому збільшення кількості ускладнень спостерігалось при збільшенні об’єму видаленої пухлини. Мабуть, у даній ситуації відбувається критичне видалення м’яких тканин, і їх залишків недостатньо для адекватних репаративних процесів.
Довжина резеційованого сегмента кістки варіювала від 90 до 340 мм. Найбільше випадків ускладнень було в групі хворих з довжиною резеційованого сегменту кістки від 150 до 250 мм — 11 (22,9 %). На нашу думку, число ускладнень залежить не від формальної довжини резеційованого сегмента кістки, а від того, якої довжини сегмент видаляється щодо довжини всієї кістки, адже довжина кісток у хворих однакового росту різна. Збільшення відсотка ускладнень спостерігалось при резекції фрагмента понад 30 % від загальної довжини кістки. На нашу думку, це пов’язано з підвищеним механічним навантаженням, що припадає на залишкову частину кістки. При такому великому дефекті кістки губляться місця прикріплення багатьох м’язів, що в нормальних умовах забезпечують стабільну роботу суглоба. На решту тканин випадає підвищене навантаження, що особливо відчутне на нижніх кінцівках і не завжди компенсується. Усе це призводить до остеопорозу кістки, порушення трофіки й виникнення різних видів нестабільності ендопротеза та гнійно–запальних ускладнень.
За нашими даними, при тривалості наркозу до 2,5 години відсоток гнійно–запальних ускладнень становив в середньому 10 %. Деяке збільшення частки гнійно–запальних ускладнень до 20 % відмічалося при подовженні операції до 3,5 години. Це може бути пов’язано з тим, що, як правило, такі випадки спостерігалися на операціях з різними технічними труднощами й непередбаченими ситуаціями.
Об’єм крововтрати під час операції теж впливав на розвиток післяопераційних гнійно–запальних ускладнень. Більшість операцій ендопротезування відбувалося з крововтратою 300–500 мл. При цьому зі збільшенням крововтрати від незначної, де частка гнійно–запальних ускладнень становила 6 %, відбувалося підвищення гнійно–запальних ускладнень пропорційно до величини втрати крові. Середня частка нагноєнь в групі хворих з крововтратою понад 500 мл становила 24,5 %.
Інфекційні ускладнення після ендопротезування є найбільш грізними. Згідно з даними літератури, частота гнійно–запальних ускладнень при встановленні онкологічних конструкцій ендопротезів становить від 10 до 19,4 % [11], що збігається з нашими результатами — 15,4 %.
Отже, ендопротезування суглобів при пухлинах кісток в комплексі з іншими методиками лікування забезпечує відновлення функції та опороспроможності кінцівки та підвищує якість життя хворого за умови відсутності післяопераційних ускладнень.
Висновки
Головними факторами у виникненні ускладнень після операцій ендопротезування у хворих з пухлинами кісток були: попередньо виконане хірургічне втручання, попередньо проведена променева терапія, локалізація пухлини, об’єм видаленої пухлини, довжина резеційованого фрагмента кістки по відношенню до довжини кістки в цілому, тривалість операції та об’єм крововтрати під час операції, конструкція ендопротеза та техніка його встановлення.
1. Алиев М.Д. Эндопротезирование как основа онкоортопедии // Саркомы костей, мягких тканей и опухоли кожи. — 2010. — № 4. — С. 7–12.
2. Амирасланов А.О. Эндопротезирование крупных костей и суставов у онкологических больных: Автореф. дис… д–ра мед. наук. — М., 2007.
3. Анализ осложнений после эндопротезирования коленного сустава по поводу опухолевых поражений (20–летний опыт) / Ф.Ю. Засульский, Т.А. Куляба, Д.А. Пташников [и др.] // Травматология и ортопедия России. — 2013. — № 4(40). — С. 24–32.
4. Бабалаев А.А., Соколовский В.А. Реэндопротезирование после органосохранных операций у больных опухолями костей // Саркомы костей, мягких тканей и опухоли кожи. — 2011. — № 3. — С. 23–28.
5. Бабоша В.А., Думанский Ю.В., Климовицкий В.Г. [и др.] Хирургия опухолей длинных костей конечностей. — Донецк: ДНМУ: ООО «Крылья», 2008. — 102 с.
6. Баранецкий А.Л. Асептическая нестабильность онкологических эндопротезов тазобедренного и коленного суставов (клинико–экспериментальное исследование): Дис… канд. мед. наук. — М., 2002. — 108 с.
7. Мачак Г.Н. Современные возможности и перспективы комбинированного лечения остеосаркомы: Автореф. дис… д–ра мед. наук. — М., 2007. — 51 с.
8. Нисиченко Д.В. Инфекционные осложнения у онкологических больных после эндопротезирования крупных суставов. Клиника, диагностика, лечение, профилактика. Автореф. дис… канд. мед. наук. — М., 2010. — 31 с.
9. Опыт использования мегапротезов в хирургическом лечении больных опухолями костей / Алиев М.Д., Нисиченко Д.В., Орехов М.Н. [и др.] // Мат–лы науч.–практ. конф. травматологов–ортопедов России с межд. участием «Актуальные проблемы костной патологии у детей и взрослых». — М., 2008. — С. 16–17.
10. Тепляков В.В., Карпенко В.Ю., Шаталов А.М. Эндопротезирование длинных костей и суставов при дефиците мягких тканей // Саркомы костей, мягких тканей и опухоли кожи. — 2011. — № 3. — С. 16–22.
11. Эндопротезирование при опухолевом поражении длинных костей / В.В. Тепляков, В.Ю. Карпенко, Г.А. Франк [и др.] // Российский педиатрический журнал. — 2009. — № 5. — С. 11–14.
12. Ahlmann E.R. Intercalary endoprosthetic reconstruction fordiaphyseal bone tumours // J. Bone Jt Surg. Br. — 2006. — Vol. 88 (11). — P. 1487–1491.
13. Alberto Pappo. Pediatric Bone and Soft Tissue Sarcomas. — Berlin; Heidelberg: Springer–Verlag, 2006. — 255 р.
14. Balsamo L.H. Distal tibial osteoarticular allografts / L.H. Balsamo, T.I. Malinin, H.T. Temple // Clin. Orthop. Relat. Res. — 2007. — Vol. 459. — P. 92–95.
15. Cemented distal femoral endoprostheses for musculoskeletal tumor: improved survival of modular versus custom implants / A.J. Schwartz, J.M. Kabo, F.C. Eilber [et al.] // Clin. Orthop. Relat. Res. — 2010. — Vol. 468(8). — P. 2198–2210.
16. Failure mode classification for tumor endoprostheses: retrospective review of five institutions and a literature review / E.R. Henderson, J.S. Groundland, E. Pala [et al.] // J. Bone Joint Surg. Am. — 2011. — Vol. 93(5). — P. 418–429.
17. Li W.C., Yang R.S., Tsauo J.Y. Knee proprioception in patients with osteosarcoma around the knee after modular endoprosthetic reconstruction // J. Bone Joint Surg. Am. — 2005. — Vol. 87(4). — P. 850–856.
18. Osteosarcoma: A multidisciplinary approach to diagnosis and treatment / J.C. Wittig, J. Bickels, D. Priebat [et al.] // Am. Fam. Physician. — 2002. — Vol. 65(6). — P. 1123–1132.
19. Proximal humerus reconstructions for tumors / B.K. Potter, S.C. Adams, J.D. Pitcher [et al.] // Clin. Orthop. Relat. Res. — 2009. — Vol. 467(4). — P. 1035–1041.
20. Reconstruction of extremity long bone defects after sarcoma resection with vascularized fibula flaps: a 10–year review / C.M. Chen, J.J. Disa, H.Y. Lee [et al.] // Plast. Reconstr. Surg. — 2007. — Vol. 119(3). — P. 915–924.
21. The Classic: amputation and adriamycin in primary osteosarcoma / Cortes E.P., Holland J.F., Wang J.J. [et al.] // Clin. Orthop. Relat. Res. — 2005. — Vol. 438. — P. 5–8.

/40/40.jpg)
/42/42.jpg)