Журнал «Травма» Том 15, №4, 2014
Вернуться к номеру
Опыт применения грязелечения у больных с травматической болезнью спинного мозга
Авторы: Каладзе Н.Н., Савелко Н.В. - ГУ «Крымский государственный медицинский университет имени С.И. Георгиевского», г. Симферополь
Рубрики: Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
В работе представлены результаты изучения влияния комплексного санаторно-курортного лечения с применением грязелечения различной площади на структурно-функциональное состояние и метаболизм костной ткани у 88 больных травматической болезнью спинного мозга. Изучены показатели ультразвуковой денситометрии, уровни кальцийрегулирующих гормонов (паратиреоидного гормона, кальцитонина, кальцитриола), уровней маркеров костного метаболизма (активности щелочной фосфатазы, остеокальцина, дезоксипиридинолина в соотношении с креатинином в моче). Установлено, что использование грязелечения большой площади в комплексном санаторно-курортном лечении больных травматической болезнью спинного мозга способствует снижению показателей ультразвуковой денситометрии, активизации костной резорбции, наиболее выраженных у пациентов с исходной остеопенией и остеопорозом.
У роботі наведені результати вивчення впливу комплексного санаторно-курортного лікування із застосуванням грязелікування різної площі на структурно-функціональний стан і метаболізм кісткової тканини у 88 хворих із травматичною хворобою спинного мозку. Вивчено показники ультразвукової денситометрії, рівні кальційрегулюючих гормонів (паратиреоїдного гормону, кальцитоніну, кальцитріолу), рівнів маркерів кісткового метаболізму (активності лужної фосфатази, остеокальцину, дезоксипіридиноліну у співвідношенні з креатиніном в сечі). Установлено, що використання грязелікування великої площі в комплексному санаторно-курортному лікуванні хворих із травматичною хворобою спинного мозку сприяє зниженню показників ультразвукової денситометрії, активізації кісткової резорбції, найбільш виражених у пацієнтів із вихідною остеопенією і остеопорозом.
The paper presents results of the studying the effect of complex sanatorium-resort treatment with mud therapy of various sizes on the structural and functional status and bone tissue metabolism in 88 patients with traumatic disease of spinal cord. We studied parameters of ultrasound densitometry, levels of calcium-regulating hormones (parathyroid hormone, calcitonin, calcitriol), levels of bone metabolism markers (activity of alkaline phosphatase, osteocalcin, deoxypyridinoline with a ratio of creatinine in urine). It is found that the use of mud therapy of a large area in complex sanatorium-resort treatment of patients with traumatic disease of spinal cord reduces the performance of ultrasonic densitometry, activation of bone resorption, the most pronounced in patients with initial osteopenia and osteoporosis.
травматическая болезнь спинного мозга, остеопороз, грязелечение.
травматична хвороба спинного мозку, остеопороз, грязелікування.
traumatic disease of spinal cord, osteoporosis, mud therapy.
Статья опубликована на с. 111-115
Травматическая болезнь спинного мозга (ТБСМ) является системным поражением всего организма, включающим в себя нарушение функции спинного мозга, а также деятельности многих внутренних органов и систем организма [4, 7]. Проблема реабилитации данной категории больных продолжает оставаться одной из самых актуальных в связи с отчетливой тенденцией к увеличению в последние десятилетия количества пострадавших в результате различных видов травматизма. Одним из клинических проявлений ТБСМ является развитие остеопороза, интенсивность выраженности которого свидетельствует о тяжести болезни, адекватности проводимого лечения и влияет на реабилитационный прогноз.
В реабилитации больных ТБСМ применяют разнообразные физические факторы, среди которых важная роль принадлежит лечебным грязям [1, 2, 5]. В механизме действия лечебных грязей лежит сложное и взаимосвязанное влияние на организм температурного, механического, химического и биологического факторов. Применение грязелечения обусловлено его клиническими эффектами: противовоспалительным, репаративно-регенераторным, дефиброзирующим, иммуностимулирующим [6, 8]. Однако остается неизученным влияние широко применяемого грязелечения на структурно-функциональное состояние костной ткани (СФС КТ) у данной категории больных.
Цель исследования: изучить влияние санаторно-курортного лечения с применением грязелечения различной площади на СФС КТ и костный метаболизм у больных ТБСМ.
Материал и методы исследования
Проведено обследование 88 больных ТБСМ мужского пола в возрасте от 22 до 43 лет, получавших лечение в специализированном спинальном санатории им. академика Н.Н. Бурденко в г. Саки. Давность заболевания составляла от 1 года до 12 лет. Поражение спинного мозга на уровне грудного отдела позвоночника было у 24 (27,3 %) больных, поясничного — у 64 (72,7 %) больных. У всех больных имела место изолированная позвоночно-спинномозговая травма с частичным повреждением спинного мозга, с неполным нарушением проводимости, по характеру повреждения — закрытая травма.
СФС КТ изучалось с помощью ультразвуковой денситометрии на аппарате Achilles+ (Lunar Corp. Madison, USA). Определяли следующие показатели: 1) скорость распространения ультразвука (СРУ, м/с); 2) широкополосное ослабление ультразвука (ШОУ, дБ/МГц); 3) индекс прочности костной ткани (ИП КТ, %). Диагноз остеопении подтверждался при значениях ИП КТ в диапазоне от –1 SD до –2,5 SD относительно нормативных показателей, диагноз остеопороза — при значениях показателя ИП КТ ниже чем –2,5 SD.
Исследовались уровни кальцийрегулирующих гормонов в сыворотке крови: паратиреоидного (ПТГ, пг/мл, реактивы I-PTH ELISA, DSL, США), кальцитонина (КТн, пг/мл, реактивы Calcitonin ELISA, BIOMERICA, США) и кальцитриола (КТр, пг/мл, реактивы 1,25 Vitamin D ELISA, Immundiagnostik, Германия). В качестве маркеров костеобразования в сыворотке крови исследовались уровни активности щелочной фосфатазы (ЩФ, мккат/л) и остеокальцина (ОК, нг/мл). Уровень ОК определялся ИФА-методом (набор N-MID Osteocalcin, Nordic Bioscience Diagnostics A/S, Канада). Активность щелочной фосфатазы определяли фотометрическим методом (набор реактивов ТОВ НВП «Филисит-Диагностика», Украина) по гидролизу 4-нитрофенилфосфата. Для оценки уровня костной резорбции в утренней моче натощак определяли уровень дезоксипиридинолина (ДПД, нмоль, набор Metra DPD EIA kit, Quidel Corporation, США) ИФА-методом в соотношении с содержанием креатинина (Кр, ммоль) в этой же порции мочи. Интерпретацию полученных результатов проводили согласно унифицированным физиологическим нормам.
Длительность лечения составила 40 дней. В зависимости от проводимого лечения больные ТБСМ (n = 88) были разделены на 2 группы, репрезентативные по возрасту, клинической характеристике и СФС КТ (по данным УЗ-денситометрии). В обеих группах проводилось общепринятое для данной категории больных лечение, которое включало: 1) полноценное сбалансированное питание с содержанием кальция 1000–1200 мг/сутки; 2) санаторно-курортный режим щадящий либо щадяще-тренирующий; 3) климатолечение; 4) лечебную гимнастику, механотерапию; 5) массаж классический спины и конечностей; 6) аппаратную физиотерапию, в том числе электростимуляцию ослабленных мышц конечностей; 7) психотерапию. С целью медикаментозной коррекции СФС КТ всем больным ТБСМ назначался кальцемин по 1 таблетке 2 раза в день (Sagmel, Inc., USA, регистр. свидетельство МЗ Украины № П.05.03/06821, № р.10.02/05389).
В I группе (n = 52) дополнительно применялось грязелечение в виде аппликаций сульфидной иловой грязи большой площади, более 50 % поверхности тела («брюки» и спина), температура грязи 38–40 °С, продолжительность процедуры 20 минут, через день, № 10–12. Во II группе (n = 36) в комплексном лечении применялись аппликации сульфидной иловой грязи небольшой площади, в виде «трусов» и ленты вдоль позвоночника, температура грязи 38–40 °С, продолжительность процедуры 15 минут, через день, № 10–12. В обеих группах применялись ректальные грязевые тампоны, температура грязи 40 °С, продолжительность процедуры 15–20 минут, через день, № 10–12.
Статистическую обработку данных проводили с помощью статистического пакета анализа данных программы Statistica version 6. Cравнение данных взаимосвязанных совокупностей проводили с использованием парного критерия Вилкоксона.
Результаты исследования и их обсуждение
Проведение УЗ-денситометрии у больных ТБСМ выявило снижение всех исследуемых показателей относительно нормативных значений для лиц данного пола и возраста. Снижение ИП КТ от –1 SD до –2,5 SD отмечалось у 51 (57,9 %) пациента, что расценивалось как остеопения. У 26 (29,5 %) больных значения ИП КТ были снижены более чем на 2,5 SD, что является характерным для остеопороза. У 11 (12,5 %) больных показатели СФС КТ находились в пределах нормативных значений.
У пациентов I группы под влиянием санаторно-курортного лечения с применением грязевых аппликаций большой площади отмечалось снижение показателей СРУ (с 1538,39 ± 3,85 м/с до 1534,54 ± 4,02 м/с; р < 0,001) и ШОУ (с 98,33 ± 1,81 дБ/МГц до 95,35 ± 1,89 дБ/МГц; р < 0,001), что обусловило достоверное снижение ИП КТ (с 76,21 ± 1,84 % до 73,13 ± 2,02 %, р < 0,001) и составило 4,04 % от исходных значений.
У больных II группы наблюдался прирост параметра СРУ (с 1536,94 ± 4,85 м/с до 1538,69 ± 4,55 м/с; р < 0,05) без значимой динамики ШОУ (с 99,17 ± 2,05 дБ/МГц до 99,50 ± 2,01 дБ/МГц), в результате ИП КТ после санаторно-курортного лечения достоверно не изменился (до лечения — 76,37 ± 2,39 %, после лечения — 77,08 ± 2,29 %).
Для оценки результатов лечения в зависимости от степени нарушений СФС КТ больные ТБСМ были разделены на следующие группы. В группы IА и IIА вошли пациенты с нормальными показателями УЗ-денситометрии, в IБ и IIБ — больные с изменениями СФС КТ в виде остеопении, в IВ и IIВ — больные с изменениями СФС КТ в виде остеопороза. В группе IА достоверной динамики показателей УЗ-денситометрии в процессе лечения не наблюдалось (табл. 1).
В то же время выявлена достоверная отрицательная динамика всех показателей УЗ–денситометрии у больных с исходно сниженными УЗ-характеристиками и, как результат, снижение ИП КТ в группах IБ (с 77,90 ± 1,15 % до 74,74 ± 1,24 %; р < 0,01) и IВ (с 61,77 ± 1,35 % до 57,64 ± 1,64 %; р < 0,05). Позитивная динамика показателя СРУ наблюдалась в группе IIБ у больных с остеопенией (с 1542,43 ± 4,77 м/с до 1545,19 ± 4,38 м/с; р < 0,05), что свидетельствовало о невыраженном положительном влиянии санаторно-курортного лечения на состояние костной ткани в данной группе.
Анализ результатов исследования показал различия в динамике уровней кальцийрегулирующих гормонов и маркеров костного ремоделирования у больных ТБСМ, зависящие от варианта санаторно-курортного лечения и исходного СФС КТ.
У больных I группы выявлено увеличение уровня ПТГ (с 42,44 ± 1,52 пг/мл до 45,10 ± 1,53 пг/мл; р < 0,01) и снижение уровня КТн (с 9,67 ± 0,66 пг/мл до 8,29 ± 0,65 пг/мл; р < 0,01) в сыворотке крови, без значимой динамики содержания КТр (с 27,75 ± 1,19 пг/мл до 24,98 ± 1,08 пг/мл). Такая динамика кальцийрегулирующих гормонов у пациентов I группы привела к увеличению показателя ДПД/Кр в моче на 29,3 % (с 5,98 ± 0,34 нмоль/ммоль до 7,73 ± 0,31 нмоль/ммоль; р < 0,001), а также к снижению содержания ОК (с 19,19 ± 0,82 нг/мл до 16,49 ± 0,62 нг/мл; р < 0,05) в сыворотке крови. Достоверных изменений активности ЩФ в сыворотке крови в результате лечения у пациентов I группы не отмечалось.
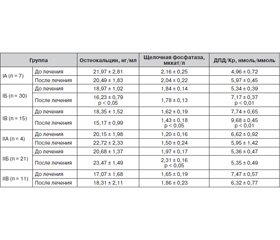
Наиболее выраженная динамика исследуемых показателей наблюдалась в группе IБ у больных с остеопенией, которая характеризовалась ростом уровня ПТГ (р < 0,01), снижением уровня КТн (р < 0,01) и сопровождалась увеличением соотношения ДПД/Кр на 34,3 % (р < 0,01), а также снижением содержания ОК (р < 0,05) в сыворотке крови (табл. 2). В группе IВ у больных с остеопорозом в результате санаторно-курортного лечения наблюдались однонаправленные достоверные изменения кальцийрегулирующих гормонов и маркеров костного метаболизма.
У больных II группы в процессе реабилитации наблюдалось достоверное увеличение содержания КТн (с 9,30 ± 0,82 пг/мл до 10,59 ± 0,67 пг/мл; р < 0,05), тенденция к повышению уровня КТр (с 26,87 ± 1,25 пг/мл до 27,70 ± 1,29 пг/мл) и снижению уровня ПТГ (с 41,86 ± 1,81 пг/мл до 40,44 ± 1,94 пг/мл) в сыворотке крови. Изменение соотношения кальцийрегулирующих гормонов явилось причиной того, что у больных данной группы на фоне повышения активности ЩФ (с 1,79 ± 0,12 мккат/л до 2,08 ± 0,13 мккат/л; р < 0,05) и стабильного уровня ОК (с 19,52 ± 0,99 нг/мл до 21,81 ± 1,16 нг/мл) в сыворотке крови уменьшилось соотношение ДПД/Кр в моче на 7,13 % (с 6,15 ± 0,37 нмоль/ммоль до 5,71 ± 0,39 нмоль/ммоль), указывающее на уменьшение костной резорбции. Более выраженные изменения изучаемых показателей в виде увеличения уровня КТн (р < 0,05) и повышения активности ЩФ (р < 0,05) в сыворотке крови наблюдались в группе IIБ у больных с остеопенией (табл. 2).
Таким образом, при проведении санаторно-курортного лечения с применением грязевых аппликаций большой площади, более 50 % поверхности тела («брюки» + спина), у больных ТБСМ наблюдалась отрицательная динамика параметров УЗ-денситометрии. Снижение ИП КТ на 4,1 % (р < 0,01) относительно первоначальных значений отмечалось у больных с остеопенией, на 6,7 % (р < 0,05) – у больных с остеопорозом. Снижение показателей УЗ-денситометрии происходило на фоне негативной динамики кальцийрегулирующих гормонов и маркеров костного метаболизма. Полученные результаты свидетельствуют о снижении активности процессов костного формирования и усилении остеорезорбции у больных I группы, выраженных как при остеопении, так и при остеопорозе. Это, по нашему мнению, являлось негативным эффектом лечения с применением грязелечения большой площади и происходило вследствие истощения адаптационных возможностей организма.
Полученные данные согласуются с данными литературы. Общеизвестно, что параметры грязелечения должны определяться в зависимости от исходного клинико-функционального состояния и индивидуальных особенностей организма [9]. Так, Г.В. Карепов (1995), анализируя результаты реабилитации спинальных больных, сделал вывод, что в лечении данной категории больных укоренилась практика применения грязей методом аппликаций, которые накладываются на часть тела, расположенную дистальнее уровня травмы. Автор считает, что так называемые «общие грязи», которые часто назначаются при травме шейного и грудного отделов позвоночника, неприемлемы у этих больных по причине наличия вялотекущих и скрытых пиелонефритов, –ослабленности и характера вегетативных расстройств [3].
В то же время у больных ТБСМ II группы, в которой применялось грязелечение небольшой площади, на сегментарно-рефлекторную зону (в виде «трусов» и ленты вдоль позвоночника), наблюдались позитивные изменения костного метаболизма, свидетельствующие об активизации процессов остеосинтеза.
Проведенные нами исследования свидетельствуют, что при назначении комплекса санаторно-курортного лечения, в том числе грязелечения, необходимо учитывать степень нарушения СФС КТ у больных ТБСМ, что может способствовать повышению эффективности реабилитации данной категории больных.
Выводы
Применение грязевых аппликаций большой площади, более 50 % поверхности тела, у больных ТБСМ сопровождается прогрессированием нарушений структурно-функционального состояния костной ткани, более выраженным при остеопении и остеопорозе, достоверным снижением индекса прочности костной ткани и негативной динамикой показателей костного метаболизма, свидетельствующей о замедлении процессов формирования и усилении резорбции костной ткани.
Комплексное санаторно-курортное лечение больных ТБСМ с применением грязевых аппликаций небольшой площади способствует активизации процессов формирования костной ткани и нормализации ее резорбции.
1. Гурленя А.М. Физиотерапия в неврологии / А.М. Гурленя, Г.Е. Багель, В.Б. Смычек. — М.: Мед. литература, 2008. — 296 с.
2. Довганюк А.П. Физиотерапия больных травматической болезнью спинного мозга / А.П. Довганюк // Физиотерапия, бальнеология и реабилитация. — 2012. — № 6. — С. 46–50.
3. Карепов Г.В. Санаторно-курортное лечение больных травматической болезнью спинного мозга / Г.В. Карепов. — Тель-Авив, 1995. — 176 с.
4. Комплексная реабилитация пациентов в промежуточном периоде позвоночно-спинномозговой травмы / В.Д. Даминов, Е.В. Зимина, О.А. Уварова, А.Н. Кузнецов // Развитие санаторно-курортной помощи, восстановительного лечения и медицинской реабилитации: тезисы Всерос. форума, Москва, 22–24 июня 2010 г. — Москва, 2010. — С. 223–224.
5. Лечебные грязи (пелоиды) Украины. Ч. 2 / Под общ. ред. М.В. Лободы, К.Д. Бабова, Т.А. Золоторевой, Е.М. Никипеловой. — К.: КИМ, 2007. — 336 с.
6. Медична реабілітація в санаторно-курортних закладах: методичний посібник: в 2 частинах. Ч. 1: Оптимізовані комплекси медичної реабілітації / За ред. Л.І. Фісенко, І.З. Самосюка. — К.: Куприянова, 2006. — С. 223–227.
7. Полищук Н.Е. Повреждения позвоночника и спинного мозга (механизмы, клиника, диагностика, лечение) / Н.Е. Полищук, Н.А. Корж, В.Я. Фищенко // Повреждения позвоночника и спинного мозга. — К.: Книга плюс, 2001. — 388 с.
8. Пономаренко Г.Н. Основы доказательной физиотерапии / Г.Н. Пономаренко. — 2-е изд., перераб. и доп. — К.: Изд-во Куприянова, 2005. — 336 с.
9. Скрипникова И. А. Реабилитация скелетно-мышечной системы при остеопорозе (обзор литературы) / И.А. Скрипникова, О. Ильич-Стоянова // Остеопороз и остеопатии. — 1999. — № 2. — С. 26–32.

/113/113.jpg)