Журнал «Травма» Том 12, №3, 2011
Вернуться к номеру
Первый клинический опыт применения обогащенного тромбоцитами фибринового геля
Авторы: Калашников А.В.1, Зубенко А.Г.1, Руденко И.А.2, Ренев К.В.2, Руденко Р.И.2, 1 ГУ «Институт травматологии и ортопедии АМН Украины», г. Киев, 2 Городская многопрофильная клиническая больница № 9, г. Запорожье
Рубрики: Травматология и ортопедия
Версия для печати
Представлен способ оптимизации репаративного остеогенеза у больных с переломами, которые осложнились несращением, с помощью обогащенного тромбоцитами фибринового геля. Полученные данные показывают его положительное влияние на сращение костей.
Репаративная регенерация, обогащенный тромбоцитами фибриновый гель, репаративный остеогенез.
Для улучшения результатов лечения, сокращения сроков нетрудоспособности и снижения процента осложнений ортопедами-травматологами осуществляется поиск новых способов влияния на течение репаративных процессов костной ткани. В настоящий момент существуют два неразрывно связанных между собой направления в изучении и усовершенствовании способов оптимизации заживления перелома. Первый направлен на усовершенствование методик оперативного лечения, способов и методов фиксации костных фрагментов, разработки новых металлоконструкций. Второй направлен на оптимизацию биологических процессов в костной мозоли, предотвращение извращенного течения репаративных процессов [1].
В последнее время большое значение уделяют использованию биологических материалов с остеоиндуктивными или остеокондуктивными свойствами для оптимизации репаративного процесса. Существует большое количество исследований, в которых использовали аутокость, аллокость, керамический гидроксиапатит и др. [2, 3], но проблема профилактики и лечения расстройств репаративного остеогенеза все еще является актуальной.
В связи с этим принципиально важным является разработка технологий оптимизации репаративного остеогенеза с использованием остеопластических материалов, которые обеспечивали бы отсутствие токсичности, бактериальную и вирусную безопасность, полную биодеградацию, биосовместимость, объединение свойств остеоиндукции и остеокондукции.
К таким биологическим материалам относится аутологический обогащенный тромбоцитами фибриновый гель (ОТФГ). ОТФГ является биологическим материалом из собственной крови больного, который можно получать даже интраоперационно. Согласно современным данным, тромбоцитарно-фибриновый гель содержит большое количество факторов роста, основные из которых:
— PDGF (тромбоцитарный фактор роста) — стимулирует реваскуляризацию, синтез коллагена, активирует макрофаги, оказывает самое высокое хемотаксическое действие из всех ростовых факторов на мезенхимальные стволовые клетки [6];
— TGF (трансформирующий фактор роста) — стимулирует синтез костной матрицы остеобластами и коллагеновой матрицы фибробластами, благодаря чему создается опора для прорастающих сосудов [7];
— FGF (фактор роста фибробластов) — принимает участие в пролиферации, дифференциации, ангиогенезе и клеточной миграции, стимулирует рост фибробластов, миобластов, остеобластов, стимулирует синтез коллагена, внеклеточного костного матрикса;
— IGF (инсулиноподобный фактор роста) — действует как митогенный фактор на остеобластную клеточную линию и как стимулятор остеогенеза на дифференцированные остеобласты [5].
ОТФГ обладает стимулирующей и остеокондуктивной способностью влияния на остеогенез за счет наличия вышеуказанных факторов роста и разветвленной сети фибриновых волокон.
Материал и методы
В 2009 г. в Запорожском межобластном центре восстановительной хирургии костей и суставов с использованием ОТФГ было проведено лечение 10 больных. Из них с несросшимися переломами костей голени было 4, с псевдоартрозами лучевой кости — 2, несросшимися переломами плечевой кости — 2, несросшимися переломами бедренной кости — 2. Из них женщин было 3, мужчин 7, средний возраст больных составил 40,2 года.
Всем больным выполнялся открытый остеосинтез по Илизарову с микрофрактурированием зоны перелома и внедрением ОТФГ. Тромбоцитарно-фибриновый гель получали у больного интраоперационно по разработанной нами методике (патент на полезную модель № 40614 «Спосіб пластики дефектів кісток»). Из кубитальной вены получали кровь объемом 10–20 мл, проводили центрифугирование крови в безвибрационной центрифуге фирмы Hettich EBA-20 в течение 12 мин со скоростью 2600 об/мин. После центрифугирования получали три фракции крови: нижняя фракция представляла собой эритроцитарную массу, верхняя фракция — бедную тромбоцитами плазму, средняя — обогащенный тромбоцитами фибриновый гель.
Анализ полученных результатов производили на основе рентгенологических снимков и средних сроков сращения переломов (приказ МЗ Украины № 189 от 09.04.2008 г. «Про затвердження положення про експертизу тимчасової непрацездатності»).
Результаты и их обсуждение
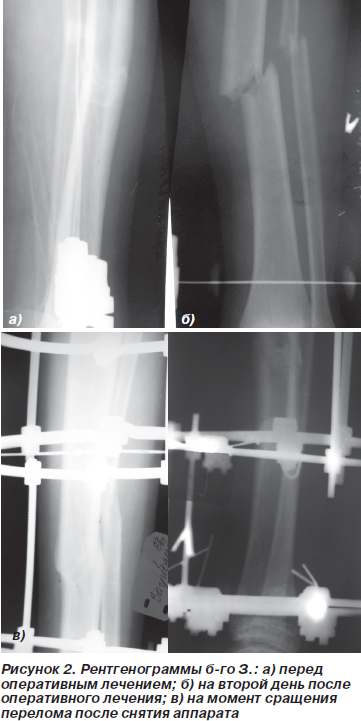
После проведенного оперативного лечения с применением ОТФГ послеоперационный период у всех больных протекал без осложнений. Рентгенологический контроль проводили на следующий день после оперативного лечения и в последующем один раз в месяц. Сразу после оперативного лечения разрешалась разработка движений в смежных суставах оперированного сегмента. В первую неделю разработка проводилась в виде пассивных укладок, со второй недели начинали активную разработку движений. Сроки сращения перелома, рентгенологические признаки сращения указаны в табл. 1.
Из приведенных выше данных видно, что использование ОТФГ положительно влияет на течение репаративного процесса перелома и, несмотря на дисрегенераторный процесс, укладывается в сроки заживления свежего перелома, не осложненного нарушением репаративной регенерации костной ткани.
Заживление операционных ран первично у всех больных. При разработке движений и увеличении нагрузки больные не отмечали выраженных болевых ощущений в зоне оперативного вмешательства. У всех наблюдаемых нами больных наступила консолидация перелома.
Оптимизация сроков сращения перелома позволила начать раннюю нагрузку на конечность, снизить риск возникновения контрактур в смежных суставах.
Клинические примеры
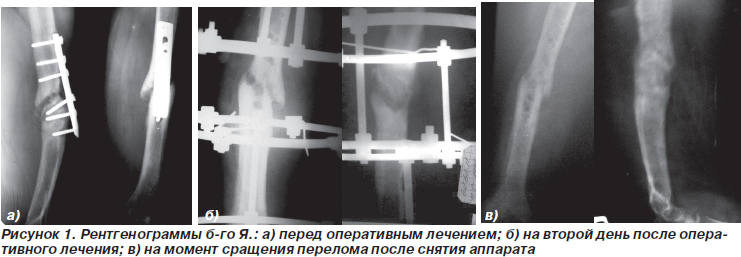
Б-й Я., 32 года, не работает, история болезни № 4056. Поступил в межобластной центр восстановительной хирургии костей и суставов с диагнозом: несросшийся перелом, инородные тела (пластина, винты) в средней трети правой плечевой кости. Из анамнеза: травма бытовая 04.10.08 г., в результате падения с высоты получил закрытый перелом правой плечевой кости. Было произведено оперативное лечение: открытая репозиция, остеосинтез накостной пластиной и кортикальными винтами. Послеоперационная рана зажила первично, без осложнений, однако при наблюдении в динамике в течение 11 мес. признаков консолидации не наблюдалось. В межобластном центре восстановительной хирургии костей и суставов 10.09.09 г. произведена операция: удаление инородных тел, открытый остеосинтез плечевой кости по Илизарову с погружением в зону перелома ОТФГ, полученного из кубитальной вены интраоперационно по вышеуказанной методике. Послеоперационный период протекал без осложнений, рана зажила первично, движения в смежных суставах начаты на второй день после операции. Признаки образования костной мозоли появились через 4 нед. после операции. Через 2,5 мес. после оперативного лечения аппарат снят (рис. 1).
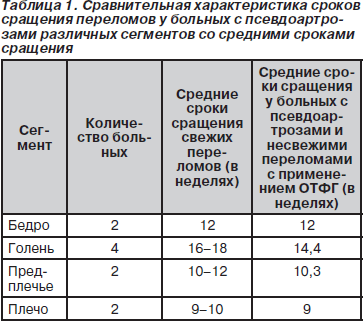
Б-й З., 16 лет, студент, история болезни № 6337. Поступил 08.12.08 г. в межобластной центр восстановительной хирургии костей и суставов с диагнозом: несросшийся перелом большеберцовой кости правой голени в нижней трети. Из анамнеза: травма 09.03.08 г. в результате падения с высоты. В течение 44 дней находился на системе постоянного скелетного вытяжения, затем фиксация гипсовой повязкой. В течение 10 мес. сращения перелома не наступило. 11.12.08 г. в межобластном центре восстановительной хирургии костей и суставов произведена операция: открытый остеосинтез костей правой голени по Илизарову с введением ОТФГ. Послеоперационный период без осложнений, рана зажила первично. С 5-го дня начата дозированная нагрузка на оперированную конечность, через 1 мес. нагрузка доведена до полной. Рентгенологический контроль осуществляли ежемесячно. Перелом сросся через 3,7 мес., аппарат снят (рис. 2).
Выводы
1. Использование ОТФГ позволяет сращивать переломы с нарушением репаративных процессов в сроки сращения свежих неосложненных переломов.
2. ОТФГ не обладает токсическими, аллергическими свойствами, не вызывает воспалительных процессов в месте перелома.
3. Внедрение ОТФГ в место перелома не связано с дополнительной массивной инвазией.
4. Получение ОТФГ не требует дорогостоящего оборудования.
5. ОТФГ может быть использован на любом сегменте конечностей.
6. Применение ОТФГ может быть перспективным и при лечении свежих переломов.
Ватников Ю.А. Структурная и функциональная организация репаративного остеогенеза у животных: Экспериментальные и клинические исследования: Дис... д-ра вет. наук. — Москва, 2004. — 395 с.
Гамрецький А.А. Активація репаративного остеогенезу при порушеннях довгих кісток: Клініко-експериментальне дослідження: Автореф. дис… канд. мед наук / А.А. Гамрецький. — Вінниця, 2004. — 19 с.
Корж Н.А. Имплантационные материалы и остеогенез. Роль оптимизации и стимуляции в реконструкции кости / Н.А. Корж, Л.А. Кладченко, С.В. Малышкина // Ортопедия, травматология и протезирование. — 2008. — № 4. — С. 5-14.
Кузьминых И.А. Хирургическое лечение радикулярных кист с использованием биокомпозиционного материала «алломатрикс-имплант» и фибрина, обогащенного тромбоцитами: Автореф. дис… канд. мед. наук / И.А. Кузьминых. — Пермь, 2008. — 22 с.
Canalis E. Insuline — like growth factor I mediates selective anabolic effects ofparathyroid hormone in bone cultures // J. Clin. Invest. — 1989. — № 83. — P. 60-5.
Johnson A., Heldin C.H., Wasteson A., Westermark B., Deuel T.F., Huang J.S. The c-sis gene encodes a precursor of the В chain of platelet-derived growth factor // Embryology Journal. — 1984. — № 3. — P. 921-8.
Kasperk C.H., Wergedal J.E., Mohan S. Interactions of growth factors present in bone matrix with bone cells effects on DNA synthesis and alkaline phosphatase // Growth Factors. — 1990. — № 3. — P. 147-158.