Журнал «Болезни и антибиотики» 2 (2) 2009
Вернуться к номеру
Приверженность к приему лекарственных средств и пути ее повышения при бактериальных инфекциях
Авторы: Березняков И.Г., Харьковская медицинская академия последипломного образования
Рубрики: Семейная медицина/Терапия, Терапия
Версия для печати
Открытие антибиотиков и внедрение их в клиническую практику, несомненно, стало одним из величайших достижений медицины XX века. Благодаря этому классу медикаментов были спасены миллионы человеческих жизней. Тем не менее и сегодня, в начале XXI века, инфекционные заболевания остаются второй по частоте причиной смерти в мире [1]. Столь неутешительное положение дел объясняется многими факторами и прежде всего — уникальностью самого класса антибиотиков.
В отличие от подавляющего большинства других медикаментов, антимикробные препараты действуют не на компоненты клеток человеческого организма (рецепторы), а на микроорганизмы. При этом каждый антибиотик уничтожает или тормозит рост и размножение всех чувствительных к нему бактерий — вне зависимости от того, повинны ли они в возникновении заболевания у пациента или нет. Поэтому формирование и совершенствование разнообразных и эффективных механизмов резистентности (устойчивости) к антибиотикам стало условием выживания микроорганизмов в изменившейся окружающей среде. Таким образом, применение антибиотиков неизбежно ведет к отбору (селекции) резистентных штаммов и видов микроорганизмов [2].
Клиническая эффективность того или иного антимикробного препарата при лечении бактериальных инфекций зависит от многих факторов. Первое, но далеко не единственное условие — природная активность выбранного антибиотика в отношении предполагаемого или установленного возбудителя. При этом приобретенная резистентность к этому препарату должна отсутствовать или быть минимально выраженной. Результаты клинических исследований свидетельствуют, что при небольшом уровне резистентности эффективность антибактериальной терапии не снижается. Однако лечение становится неэффективным, когда количество резистентных штаммов превышает некий пороговый уровень. Например, для внебольничных пневмококковых инфекций этот показатель составляет примерно 20–30 % [3].
Вовторых, антибиотик следует назначать в адекватной дозе, что требует знания фармакокинетических и фармакодинамических характеристик препарата. Все антибиотики можно разделить на дозозависимые и времязависимые. Если антибактериальная активность антимикробного препарата зависит от его концентрации в очаге воспаления (так называемые дозозависимые антибиотики), то наилучшего эффекта можно добиться при использовании высоких доз препарата, близких к токсическим [4]. При этом чем выше отношение максимальной (пиковой) концентрации антибиотика в плазме к величине минимальной подавляющей концентрации (МПК) возбудителя заболевания, тем лучше. Фторхинолоны вместе с аминогликозидами, амфотерицином B и метронидазолом входят в группу дозозависимых антимикробных средств.
В последние годы было показано, что предсказать эффективность дозозависимого антибиотика можно с помощью еще одного фармакодинамического параметра — отношения площади под фармакокинетической кривой (AUC), отражающей изменение концентрации препарата за время после его введения, к МПК (или минимальной бактерицидной концентрации). При прочих равных условиях чем выше AUC/МПК, тем эффективнее препарат.
Эффективность второй группы антибиотиков, представленных βлактамами, гликопептидами, макролидами (кроме азитромицина и, возможно, кларитромицина), клиндамицином, зависит не столько от максимальной концентрации в плазме крови или AUC, сколько от промежутка времени, в течение которого концентрация препарата в крови превышает МПК возбудителя заболевания. Так, для реализации антибактериального эффекта βлактамов необходимо, чтобы их концентрация в крови превышала МПК возбудителя в течение не менее 40 % интервала времени между введениями очередных доз антибиотика.
Клиническое значение фармакодинамических показателей можно проиллюстрировать на примере аминогликозидов и βлактамов. Применение современных знаний о фармакодинамике аминогликозидов позволило разработать и внедрить новые подходы к их дозированию. Однократное внутривенное введение всей суточной дозы гентамицина, амикацина и других аминогликозидов постепенно вытесняет традиционное 2–3разовое введение. Напротив, особенности фармакодинамики βлактамов могут повлечь за собой пересмотр кратности применения некоторых из них в сторону увеличения.
Втретьих, длительность курса антибактериальной терапии должна быть оптимальной. Досрочное прекращение лечения может увеличить сроки выздоровления, в то время как избыточное по времени назначение антибиотиков сопровождается возрастанием частоты нежелательных лекарственных явлений (НЛЯ) и повышенным риском селекции резистентности.
Клиническая эффективность антибиотика будет зависеть и от фармакокинетических параметров (например, способности препарата проникать в очаг инфекции известной локализации и накапливаться там), состояния собственных защитных сил макроорганизма и других факторов [5]. Наконец, очень важна точность соблюдения пациентом предписанного режима дозирования.
Для характеристики приема медикаментов пациентами используют разные определения. Чаще всего говорят либо о комплайентности, либо о приверженности к лечению, хотя ни один из этих терминов не является оптимальным. К недостаткам термина «комплайентность» можно отнести то, что он указывает на пассивное выполнение больным назначений врача и на тот факт, что план лечения не был согласован врачом с пациентом. Приверженность к лечению — термин более гибкий и позволяет оценивать долю от выписанных доз медикаментов, которые действительно были приняты пациентом за определенный промежуток времени. При желании можно учитывать также сведения о приеме (принимались ли ежедневно все выписанные таблетки?) и времени приема лекарств (принимались ли медикаменты в указанные промежутки времени?) [6].
Приверженность к лечению обычно выше при острых состояниях, включая бактериальные инфекции. При хронических заболеваниях она значительно снижается спустя 6 мес. лечения [7–9]. Обычно приверженность к лечению выше во время рандомизированных клинических исследований (РКИ), чем в рутинной клинической практике, хотя при хронических заболеваниях она может не превышать 48–73 % [8, 10, 11].
Низкая приверженность к лечению — далеко не безобидное явление. Например, в США от 33 до 69 % всех госпитализаций, связанных с медикаментами, обусловлены низкой приверженностью к лечению, что обходится стране приблизительно в 100 млрд долларов в год [12–15].
При высокой приверженности к приему антибиотиков больные раньше выздоравливают и у них реже бывают рецидивы бактериальных инфекций. Например, в одной из работ, опубликованных еще в середине 70х гг. прошлого века, была проанализирована зависимость частоты рецидивов инфекций мочевых путей у детей от приверженности к лечению [16]. Оказалось, что при неполной приверженности к терапии (пациентов и/или их родителей или опекунов) частота рецидивов в течение года была в 1,6 раза, а при полной некомплайентности — в 2,4 раза выше, чем при полной приверженности к лечению (рис. 1).
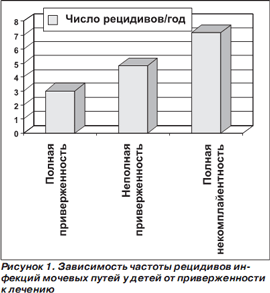
Интересные данные получены в недавнем метаанализе связи между приверженностью к лекарственной терапии и смертностью [17]. В окончательный анализ были включены 21 РКИ (46 847 пациентов), в том числе 8 РКИ с группой плацебо (19 633 больных), проведенных в 1970–2005 гг. у постинфарктных больных, больных СПИДом, у лиц с гиперхолестеринемией, сердечной недостаточностью, у пациентов после трансплантации сердца, больных с сахарным диабетом, а также исследования, посвященные первичной профилактике сердечнососудистых заболеваний. При этом в 2 РКИ у больных с аритмиями и сахарным диабетом (768 пациентов) активное лечение повышало риск смерти по сравнению с плацебо. Результаты метаанализа представлены на рис. 2.
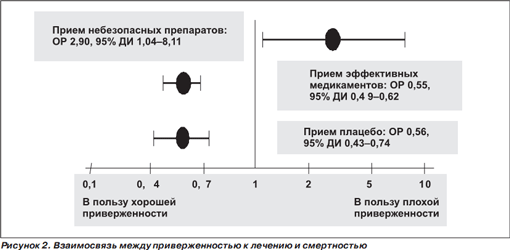
Было продемонстрировано, что хорошая приверженность к приему эффективных медикаментов ассоциируется со снижением смертности. Более того, установление связи между хорошей приверженностью к приему плацебо и смертностью указывает на существование эффекта «здорового приверженца». Таким образом, хорошая приверженность к лекарственной терапии может быть суррогатным маркером «здорового поведения» (overall healthy behaviour).
С другой стороны, приверженность к приему небезопасных препаратов ассоциировалась с увеличением смертности. Авторы метаанализа высказали предположение, что стратификация больных в РКИ по приверженности к лечению может облегчить выявление небезопасных/вредных медикаментов, если частота НЛЯ окажется выше в группе пациентов с высокой приверженностью к приему лекарств [17].
Плохая (низкая) приверженность к приему медикаментов может быть намеренной и непреднамеренной. В первом случае больной осознанно отказывается от приема лекарств. Причины могут быть самыми разными: финансовыми (невозможность приобретения выписанного препарата изза отсутствия средств), личностными (ощущение себя выздоровевшим или здоровым либо безразличное отношение к своему здоровью) и т.д. Непреднамеренный пропуск приема очередной дозы препарата чаще всего связан с забывчивостью или затруднениями при приеме медикамента изза неудобной упаковки или формы выпуска. Когда самих пациентов спрашивают о причинах несоблюдения предписанного режима лечения, они чаще всего ссылаются на забывчивость либо вовсе не дают вразумительного ответа (рис. 3) [18].
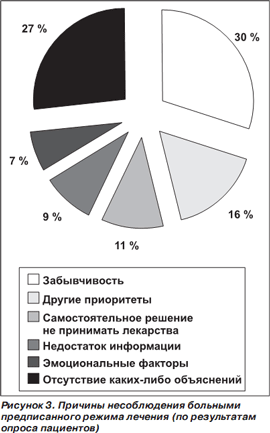
Вопреки распространенным заблуждениям низкая приверженность к терапии не связана ни с возрастом, ни с полом больного, ни с его семейным или социальным положением, уровнем образования, доходами, ни даже со стоимостью препарата или отсутствием необходимости платить за лекарство [19]. Приверженность к приему лекарств — будь она высокой или низкой — является одной из черт личности человека.
Во время лечения антибиотиками многие пациенты допускают ошибки. Одной из наиболее распространенных является пропуск приема очередной дозы антибиотика. Пропуск может быть непреднамеренным и намеренным — например, изза опасений взаимодействия антибиотика с другими медикаментами или с алкоголем. Другой ошибкой является прием дополнительных доз антибиотика, особенно в начале лечения. Возможными причинами могут быть тяжесть симптомов заболевания или желание добиться скорейшего улучшения. В ряде случаев пациенты досрочно прекращают прием лекарств, например, изза наступления субъективного улучшения до завершения предписанного курса терапии. Типичный пример — прекращение болей при мочеиспускании и других дизурических явлений у пациенток с неосложненным циститом на 2й день лечения, что влечет за собой отказ от дальнейшего приема антибиотиков, хотя длительность антибактериальной терапии в подобных случаях составляет обычно 3 суток. Среди других причин досрочного прекращения лечения можно упомянуть возникновение побочных эффектов в процессе лечения, затруднения при проглатывании или неприемлемые для больного органолептические свойства таблеток (неприятный вкус или запах), «обманутые ожидания» — отсутствие значительного улучшения в ожидавшиеся пациентом сроки и т.д.
Иногда больные самостоятельно изменяют режим дозирования (например, принимают антибиотик 2 раза в сутки вместо 3). Одной из причин такой «самодеятельности» может быть несовпадение режима дозирования с образом жизни пациента. Некоторые больные отказываются от приобретения антибиотика по экономическим соображениям или опасаясь негативного воздействия препарата на желудочнокишечный тракт, иммунную систему.
Встречаются и случаи задержки с началом лечения, например, в связи с надеждой на самостоятельное разрешение инфекции без приема антибиотика [19].
Можно выделить несколько подходов к повышению приверженности к терапии. Прежде всего это уменьшение кратности приема антибиотиков [19, 20]. В систематическом обзоре 76 исследований, в которых для оценки приверженности к приему лекарств использовали электронные мониторы, показано, что при назначении лекарств 1 раз в сутки приверженность к лечению статистически значимо выше, чем при назначении 3 или 4 раза в сутки (рис. 4) [11]. Однако однократный прием препаратов с точки зрения приверженности к терапии не превосходил двукратный.

Напротив, в более позднем метаанализе, в который были включены проспективные рандомизированные и когортные исследования и ретроспективные обзоры медицинских записей и баз данных, показано, что при назначении медикамента 1 раз в сутки приверженность к лечению статистически значимо превосходила таковую при назначении препарата 2 раза в сутки [21]. Авторы рекомендаций по вопросам приверженности к приему медикаментов сочли эти данные неубедительными [20].
С другой стороны, хотя в метаанализ в подавляющем большинстве случаев включали исследования у больных с хроническими заболеваниями, результаты исследований с антибиотиками, как правило, согласуются с его результатами.
Например, приверженность к лечению у пациентов врачей общей практики была самой высокой при 1кратном приеме антибиотика в сутки и снижалась по мере увеличения кратности приема препаратов (рис. 5). К недостаткам этого исследования следует отнести тот факт, что разными были не только кратность приема, но и сами тестировавшиеся антибиотики [21].
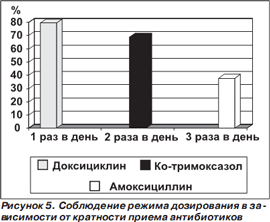
Этого недостатка лишено недавнее проспективное рандомизированное одноцентровое исследование. 122 амбулаторных больных с обострениями хронического бронхита были рандомизированы в 2 группы [23]. Пациенты первой группы получали кларитромицин в стандартной дозе 250 мг 2 раза в сутки, второй группы — кларитромицин в лекарственной форме с постепенным высвобождением антибиотика по 500 мг 1 раз в сутки. Длительность терапии в обеих группах была одинаковой — 7 суток.
Приверженность терапии (комплайентность) оценивалась с помощью электронного мониторирования приема медикаментов. В окончательный анализ вошли 119 человек (58 — в группе 1кратного приема, 61 — в группе 2кратного приема). Приверженность лечению по всем изученным параметрам была выше в группе 1кратного приема антибиотика: общая комплайентность (93,7 % по сравнению с 81,3 % в группе 2кратного приема, р < 0,0001), количество дней, на протяжении которых больные принимали все предписанные дозы антибиотиков (80,3 % по сравнению с 68,6 %, р < 0,0001), должные интервалы между приемом очередных доз (74,4 % по сравнению с 56,4 %, р < 0,001), средние интервалы между приемом очередных доз (95,6 % по сравнению со 106,3 % от ожидавшихся величин, р < 0,001) [22].
Таким образом, даже несмотря на непродолжительный срок антибактериальной терапии, комплайентность была выше в случае приема антибиотика 1 раз в день. Этот эффект наблюдался как по отношению к дозам препарата, так и ко времени его приема. Следовательно, назначение антибиотиков 1 раз в сутки предпочтительно при инфекциях дыхательных путей.
Невозможно пройти мимо того факта, что внедрение новых технологий производства антибиотиков позволяет существенно повысить приверженность к терапии. Например, традиционная схема дозирования кларитромицина, офлоксацина, ципрофлоксацина предполагает прием антибиотиков внутрь 2 раза в сутки. Создание новых лекарственных форм этих препаратов (таблетки OD (once daily, то есть один раз в день) и др.) дает возможность принимать суточную дозу препаратов однократно. Причем современные технологические достижения распространяются не только на дозозависимые антибиотики.
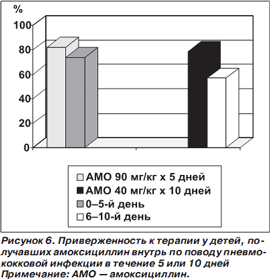
Следующий подход к улучшению приверженности к лечению — сокращение продолжительности терапии. В одном из исследований сравнивали приверженность к лечению у детей с пневмококковыми инфекциями при 5 и 10дневных курсах приема амоксициллина (рис. 6). Неудивительно, что она была выше при кратком курсе. Интересно другое: при 10дневном курсе приверженность в первые 5 дней лечения оказалась выше, чем с 6го по 10й день терапии [24].
Сокращение продолжительности антибиотикотерапии ни в коем случае не должно приводить к ухудшению эффективности лечения. В последние годы накапливаются данные о высокой эффективности кратких курсов применения антибиотиков, по крайней мере при внебольничных инфекциях дыхательных путей. Например, была продемонстрирована сопоставимая эффективность 5дневной антибиотикотерапии левофлоксацином в дозе 750 мг/сут и стандартного 10дневного курса лечения тем же антибиотиком по 500 мг/сут у больных с внебольничными пневмониями [24]. Обнадеживающие результаты получены еще в одном РКИ. 119 госпитализированных взрослых больных со среднетяжелой внебольничной пневмонией (количество баллов по шкале PSI Ј 110), у которых после 3дневной внутривенной терапии амоксициллином наступило существенное улучшение, были рандомизированы в группы дальнейшего лечения в течение 5 дней амоксициллином по 750 мг 3 раза в сутки внутрь или плацебо. В исследование не включали больных с иммунодефицитами и со значительным выпотом в плевре. Частота клинического и рентгенологического излечения в обеих группах не различалась ни спустя 10 дней от начала терапии, ни через 28 дней от начала лечения [26]. В случае подтверждения полученных результатов в последующих исследованиях рекомендации по длительности антибактериальной терапии могут быть пересмотрены.
Возможность совмещения минимальной кратности приема с сокращением продолжительности терапии можно проиллюстрировать на примере азитромицина. При нетяжелых внебольничных инфекциях дыхательных путей этот антибиотик назначается внутрь по 500 мг 1 раз в сутки сроком на 3 дня.
Повышению приверженности к приему антибиотиков будет способствовать также выбор приемлемой для пациента или его родителей лекарственной формы либо упаковки препарата. Например, по технологическим причинам невозможно разместить 1 г амоксициллина в одной таблетке и при этом сделать ее небольшой и удобной для проглатывания. Появление новых технологий (Солютаб и др.) позволяет преодолеть это затруднение. Амоксициллин в форме Солютаб (хоть 1 г, хоть больше) можно растворить в воде и полученный раствор с приятным вкусом и запахом принимать внутрь без какихлибо неудобств.
Еще один подход к повышению приверженности — выведение на рынок медикаментов с улучшенной переносимостью. Например, высокоэффективный противогрибковый антибиотик амфотерицин В плохо переносится больными, что в ряде случаев приводит к отказам от продолжения лечения этим препаратом. Появление липосомальной лекарственной формы амфотерицина В позволяет существенно снизить остроту этой проблемы, хотя и не устранить ее целиком.
Важное значение придается выдаче пациенту (либо его родственникам и/или опекунам) письменных инструкций по приему антибиотиков. Для большинства немедицинского населения как международное, так и торговое название медикаментов — не более чем набор звуков. Названия препаратов, как и рекомендации по их приему, зачастую просто не откладываются в памяти. Письменные инструкции позволяют отчасти преодолеть эту проблему. Они приобретают особую актуальность, когда речь идет о больных пожилого и старческого возраста, пациентах со сниженной памятью или интеллектом.
Среди других методов повышения приверженности к терапии обычно упоминают обучение больного, а также использование разных форм напоминания о времени приема очередной дозы. Это важные аспекты работы врача, но, как представляется, значимость их в случаях непродолжительной антибактериальной терапии переоценивать не следует.
Заключение
Для характеристики приема пациентами лекарственных средств нередко используют термин «приверженность к лечению», позволяющий оценивать долю от выписанных доз медикаментов, которые действительно были приняты пациентом за определенный промежуток времени. В рамках этого термина можно также учитывать сведения о приеме (принимались ли ежедневно все выписанные таблетки?) и времени приема лекарств (принимались ли медикаменты в указанные промежутки времени?).
Приверженность к лечению обычно выше при острых состояниях, включая бактериальные инфекции. Высокая приверженность к приему антибиотиков ассоциируется с повышением эффективности вмешательства.
Плохая (низкая) приверженность к приему медикаментов может быть намеренной и непреднамеренной. В первом случае больной осознанно отказывается от приема лекарств по финансовым, личностным и другим причинам. Непреднамеренный пропуск приема очередной дозы препарата чаще всего связан с забывчивостью или затруднениями при приеме медикамента изза неудобной упаковки или формы выпуска.
Низкая приверженность к терапии не связана ни с возрастом, ни с полом больного, ни с его семейным или социальным положением, уровнем образования, доходами, ни даже со стоимостью препарата или отсутствием необходимости платить за лекарство. Приверженность к приему лекарств — будь она высокой или низкой — является одной из черт личности человека.
Существует несколько подходов к повышению приверженности к приему антибиотиков при бактериальных инфекциях. Степень научной обоснованности каждого из них весьма различается. Наиболее известными и изученными являются: 1) уменьшение кратности приема антибиотиков; 2) сокращение продолжительности терапии; 3) выбор приемлемой для пациента или его родителей лекарственной формы либо упаковки препарата; 4) выведение на рынок медикаментов с улучшенной переносимостью; 5) выдача пациенту (либо его родственникам и/или опекунам) письменных инструкций по приему антибиотиков; 6) обучение больного; 7) использование разных форм напоминания о времени приема очередной дозы.
1 The world health report 2000 — health systems: improving performance. — Geneva: WHO, 2000.
2. Березняков И.Г. Резистентность к антибиотикам: механизмы возникновения и клиническое значение. — 2006. — 72 с.
3. Яковлев С.В. Стратегия применения антибиотиков в стационаре // Клин. антибиотикотер. — 2001. — № 5–6. — С. 3-10.
4. Blondeau J.M. Why agents may fail — and how to improve results in RTI // Consultant. — 2000. — Vol. 40 (Suppl. 13. Respiratory tract infections: is «first-line» therapy now second best?). — Р. S5-S12.
5. Towner K.J. The problem of resistance // Antimicrobial chemotherapy. // Greenwood D., editor. 4th ed. — Oxford; New York: Oxford University Press, 2001. — Р. 137-144.
6. Osterberg L., Blaschke T. Adherence to medication // N. Engl. J. Med. — 2005. — Vol. 353. — Р. 487-497.
7. Jackevicius C.A., Mamdani M., Tu J.V. Adherence with statin therapy in elderly patients with and without acute coronary syndromes // JAMA. — 2002. — Vol. 288. — Р. 462-467.
8. Cramer J., Rosenheck R., Kirk G., Krol W., Krystal J. Medication compliance feedback and monitoring in a clinical trial: predictors and outcomes // Value Health. — 2003. — Vol. 6. — Р. 566-573.
9. Haynes R.B., McDonald H.P., Garg A.X. Helping patients follow prescribed treatment: clinical applications // JAMA. — 2002. — Vol. 288. — Р. 2880-2883.
10. Waeber B., Leonetti G., Kolloch R., McInnes G.T. Compliance with aspirin or placebo in the Hypertension Optimal Treatment (HOT) study // J. Hypertens. — 1999. — Vol. 17. — Р. 1041-1045.
11. Claxton A.J., Cramer J., Pierce C. A systematic review of the associations between dose regimens and medication compliance // Clin. Ther. — 2001. — Vol. 23. — Р. 1296-1310.
12. McDonnell P.J., Jacobs M.R. Hospital admissions resulting from preventable adverse drug reactions // Ann. Pharmacother. — 2002. — Vol. 36. — Р. 1331-1336.
13. Senst B.L., Achusim L.E., Genest R.P. et al. Practical approach to determining costs and frequency of adverse drug events in a health care network // Am. J. Health Syst. Pharm. — 2001. — Vol. 58. — Р. 1126-1132.
14. Levy G., Zamacona M.K., Jusko W.J. Developing compliance instructions for drug labeling // Clin. Pharmacol. Ther. — 2000. — Vol. 68. — Р. 586-591.
15. Berg J.S., Dischler J., Wagner D.J., Raia J.J., Palmer-Shevlin N. Medication compliance: a healthcare problem // Ann. Pharmacother. — 1993. — Vol. 27, suppl. 9. — Р. S1-S24.
16. Daschner F., Marget W. Treatment of recurrent urinary tract infection in children. II. Compliance of parents and children with antibiotic therapy regimen // Acta Paediatrica Scandinavica. — 1975. — Vol. 64. — Р. 105-8.
17. Simpson S.H., Eurich D.T., Majumdar S.R., Padwal R.S., Tsuyuki R.T., Varney J. et al. A meta-analysis of the association between adherence to drug therapy and mortality // BMJ. — 2006. — Vol. 333, № 7557. — Р. 15-20.
18. Patient compliance in medical practice and clinical trials // Cramer J.A., Spilker B. eds. — New York: Raven Press, 1991. — Р. 387-92.
19. Kardas P. Patient compliance with antibiotic treatment for respiratory tract infections // J. Antimicrob. Chemother. — 2002. — Vol. 49. — Р. 897-903.
20. Nunes V., Neilson J., O’Flynn N., Calvert N., Kuntze S., Smithson H. et al. Clinical guidelines and evidence review for medicines adherence: involving patients in decisions about prescribed medicines and supporting adherence. — London: National Collaborating Centre for Primary Care and Royal College of General Practitioners, 2009. — 364 р.
21. Iskedjian M. et al. Relationship between daily dose frequency and adherence to antihypertensive pharmacotherapy: evidence from a meta-analysis // Clin. Ther. — 2002. — Vol. 24, № 2. — Р. 302-316.
22. Cockburn J., Reid A.L., Bowman J.A., Sanson-Fisher R.W. Effects of intervention on antibiotic compliance in patients in general practice // Med. J. Aust. — 1987. — Vol. 147. — Р. 324-328.
23. Kardas P. Comparison of patient compliance with once-daily and twice-daily antibiotic regimens in respiratory tract infections: results of a randomized trial // J. Antimicrob. Chemother. — 2007. — Vol. 59, № 3. — Р. 531-536.
24. Schrag S. J., Pena C., Fernandez J., Sanchez J., Gomez V., Perez E. et al. Effect of short-course, high-dose amoxicillin therapy on resistant pneumococcal carriage: a randomized trial // J. Am. Med. Ass. — 2001. — Vol. 286. — Р. 49–56.
25. Dunbar L.M., Wunderink R.G., Habib M.P., Smith L.G., Tennenberg A.M., Khashab M.M. et al. High-dose, short-course levofloxacin for community-acquired pneumonia: a new treatment paradigm // Clin. Infect. Dis. — 2003. — Vol. 37. — Р. 752-60.
26. El Moussaoui R., de Borgie C.A.J.M., van den Broek P., Hustinx W.N., Bresser P., van den Berk G.E.L. et al. Effectiveness of discontinuing antibiotic treatment after three days versus eight days in mild to moderate-severe community acquired pneumonia: randomised, double blind study // BMJ. — 2006. — Vol. 332. — Р. 1355.
